Witamy w sekcji informacyjnej Dr. Galva
Tutaj znajdziesz odpowiedzi na najczęściej zadawane pytania dotyczące galwaniki. Niezależnie od tego, czy chcesz dowiedzieć się więcej o naszych produktach, czy o procesie zamówienia – na tej stronie znajdziesz wyczerpujące informacje. Jeśli jednak masz pytanie, na które nie znalazłeś tu odpowiedzi, nie wahaj się z nami skontaktować.
Przewodnik po galwanizacji znajdziesz tutaj:
Jeżeli interesują Cię informacje o najnowszych osiągnięciach lub inne publikacje, zajrzyj do sekcji „Publikacje”: Publikacje
- Czym się różni oksydowanie od patynowania?
-
Różnica między oksydowaniem a patynowaniem polega na zastosowanych metodach, materiałach i efektach końcowych, choć oba procesy mają na celu uzyskanie ochronnej lub dekoracyjnej powierzchni metalu:
Oksydowanie:
- Proces: Chemiczna obróbka, w której żelazo lub stal reagują z utleniającymi odczynnikami, tworząc czarną lub ciemnoniebieską warstwę tlenkową.
- Materiały: Stosowane typowo do stali i żelaza.
- Efekt końcowy: Ciemna, matowa lub lekko błyszcząca powierzchnia, która pełni funkcję ochrony przed korozją i jednocześnie wygląda estetycznie.
- Zastosowanie: Często w broni, narzędziach i innych stalowych częściach, aby je chronić i nadać im ciemną optykę.
Patynowanie:
- Proces: Chemiczny lub naturalny, w którym metale takie jak miedź, brąz czy mosiądz ulegają utlenieniu i tworzą kolorową warstwę (patynę).
- Materiały: Przede wszystkim miedź, brąz i mosiądz.
- Efekt końcowy: Często zielone, niebieskie lub brązowe odcienie (np. znana zielona patyna na miedzianych dachach), zwykle dekoracyjne i dodatkowo ochronne.
- Zastosowanie: Szeroko w sztuce, rzeźbie i architekturze, aby uzyskać antyczny lub estetycznie postarzały wygląd powierzchni.
Podsumowanie: oksydowanie stosuje się głównie do stali, aby uzyskać ciemną, funkcjonalną warstwę ochronną, natomiast patynowanie dotyczy miedzi i pokrewnych metali w celu uzyskania dekoracyjnej, barwnej powierzchni.
- Jak wyczernić mosiądz? Jakie produkty Państwo polecają?
-
Do czernienia mosiądzu najlepiej nadaje się patynowanie. Żel patynujący Nero został opracowany specjalnie po to, aby nadać mosiądzowi ciemną powierzchnię. Jest prosty w użyciu i zapewnia trwałą, dekoracyjną patynę.
Po rozcieńczeniu można także bardzo dobrze uzyskać odcienie brązu.
- Czym różnią się oksydy?
-
Produkty do oksydowania Dr. Galva różnią się przede wszystkim sposobem aplikacji oraz typowymi zastosowaniami. Poniżej najważniejsze różnice między trzema rodzajami:
Ultra‑3 Oksydowanie zanurzeniowe
- Zastosowanie: Metoda idealna do jednoczesnej obróbki wielu detali lub elementów o złożonych kształtach, gdzie wymagana jest równomierna warstwa. Cały detal zanurza się w roztworze oksydy.
- Zalety: Zapewnia równomierną, ciągłą warstwę oksydy także w trudno dostępnych miejscach. Szczególnie polecana do większych detali i zastosowań warsztatowych/produkcyjnych.
- Obszary użycia: Optymalna do oksydowania stalowych części w produkcji seryjnej lub tam, gdzie trzeba obrabiać wiele elementów naraz.
Ultra‑5 Szybka oksyda
- Zastosowanie: Uniwersalny preparat, który można stosować zarówno w kąpieli zanurzeniowej, jak i przez proste nanoszenie. Nadaje się do szerokiej gamy materiałów i detali.
- Zalety: Duża elastyczność aplikacji i świetne rozwiązanie „all‑round” do różnych zadań. Łatwy w użyciu, bez specjalistycznego wyposażenia.
- Obszary użycia: Idealny dla rzemieślników i majsterkowiczów szukających wszechstronnej oksydy – do małych i dużych elementów.
Ultra‑7 Oksyda do nanoszenia pędzlem
- Zastosowanie: Roztwór nanosi się bezpośrednio na powierzchnię detalu, np. pędzlem lub tamponem. Metoda szczególnie dobra do mniejszych pól lub poprawek.
- Zalety: Precyzyjna, kontrolowana aplikacja – idealna do napraw oraz detali, których nie można całkowicie zanurzyć. Szybka i prosta, także „na miejscu”.
- Obszary użycia: Do mniejszych projektów, renowacji lub odświeżania istniejącej oksydy. Sprawdza się, gdy trzeba obrobić tylko wybrane obszary bez traktowania całego detalu.
Podsumowanie:
- Oksydowanie zanurzeniowe: Do równomiernych, pełnych powłok na wielu lub dużych detalach.
- Szybka oksyda: Wszechstronna – w kąpieli lub przez nanoszenie – do różnych materiałów.
- Oksyda do nanoszenia pędzlem: Precyzyjna i prosta aplikacja na małych powierzchniach lub do poprawek.
Każdy z tych rodzajów oksydy Dr. Galva ma swoje specyficzne zalety i jest zoptymalizowany pod konkretne zastosowania, dzięki czemu możesz dobrać właściwą metodę do danego zadania.
Preparaty do oksydowania Dr. Galva są opracowane specjalnie do stali, żelaza i żeliwa. Istnieją też preparaty do barwienia stopów takich jak miedź czy mosiądz – to jednak zalicza się do patynowania. - Jaki olej po oksydowaniu?
-
Po oksydowaniu zaleca się użycie specjalnego oleju antykorozyjnego opracowanego do oksydowanych powierzchni. Oto kilka opcji:
-
Specjalne oleje do oksydy: Te oleje są opracowane do uszczelniania i ochrony oksydowanych powierzchni. Zapewniają wysoki poziom ochrony przed korozją i utrzymują czarną warstwę.
-
Olej do broni: Olej stosowany do pielęgnacji broni palnej to dobry wybór. Został zaprojektowany, by chronić metal przed korozją, dlatego znakomicie sprawdza się również na elementach po oksydowaniu.
-
Olej lniany: Naturalną ochronę zapewnia także olej lniany, który tworzy cienką warstwę ochronną i podkreśla oksydę. Jest jednak mniej trwały niż produkty specjalistyczne.
-
Olej mineralny: Lekki olej mineralny można zastosować, gdy nie ma pod ręką oleju dedykowanego do oksydy. Daje podstawową ochronę przed wilgocią, ale zwykle jest mniej skuteczny niż rozwiązania specjalistyczne.
Ważne, aby nakładać olej równomiernie, cienką warstwą, a po kilku minutach usunąć nadmiar, aby powierzchnia nie była lepka.
-
- Jak suszyć po oksydowaniu?
-
Osusz elementy bezpośrednio po oksydowaniu czystą, niepylącą ściereczką, w przeciwnym razie może pojawić się korozja.
Odnośnie czasu oczekiwania po oksydowaniu: ważne jest, aby proces oksydowania był całkowicie zakończony, a powierzchnia sucha, zanim rozpoczniesz lakierowanie. Zazwyczaj wystarcza krótki czas oczekiwania około 30 minut do 1 godziny, aby upewnić się, że powierzchnia jest stabilna. Jeśli wilgotność powietrza jest wysoka, warto poczekać nieco dłużej lub ostrożnie podgrzać elementy, aby przyspieszyć suszenie.
- Czy olejowanie oksydowanych elementów jest konieczne, jeśli później będą lakierowane?
-
Olejowanie oksydowanych elementów służy przede wszystkim dodatkowemu zabezpieczeniu przed korozją, uszczelniając powierzchnię i chroniąc ją przed wilgocią. Jeśli jednak po oksydowaniu planujesz lakierować blachy metalowe lakierem bezbarwnym, olejowanie rzeczywiście można pominąć, ponieważ warstwę ochronną zapewni lakier.
Dodatkowo lakier nie będzie dobrze przylegał do zaoliwionej powierzchni.
- Jak skuteczna jest ochrona antykorozyjna oksydy?
-
Ochrona antykorozyjna uzyskana w wyniku oksydowania jest ograniczona i zazwyczaj zapewnia jedynie umiarkowaną odporność na rdzę. Szybka oksyda tworzy na powierzchni metalu cienką, czarną warstwę tlenkową, która w pewnym stopniu chroni przed korozją, jednak nie tak skutecznie jak grubsza, przemysłowa oksyda lub pełnowartościowa powłoka ochronna.
Czynniki wpływające na ochronę przed korozją:
-
Grubość warstwy: Ponieważ warstwa tlenkowa powstała po oksydowaniu jest stosunkowo cienka, zapewnia jedynie powierzchniową ochronę.
-
Warunki środowiskowe: W wilgotnym lub agresywnym środowisku, np. w atmosferze zasolonej, sama oksyda często nie wystarcza i może szybko zawieść, jeśli powierzchnia nie zostanie dodatkowo zabezpieczona.
-
Obróbka końcowa: Skuteczność ochrony można wyraźnie poprawić, jeśli po oksydowaniu powierzchnię pokryje się odpowiednim olejem antykorozyjnym. Taka obróbka uszczelnia powierzchnię i chroni ją przed wilgocią oraz innymi czynnikami korozyjnymi.
Podsumowanie:
Bez obróbki końcowej oksydowanie zapewnia jedynie ograniczoną ochronę i nadaje się głównie do zastosowań dekoracyjnych lub tymczasowych. Dla długotrwałej ochrony, zwłaszcza w wymagającym środowisku, konieczne jest wykończenie olejem lub inną powłoką ochronną.
-
- Anoda prętowa czy płaska – która jest właściwa?
-
Wybór pomiędzy anodą prętową a anodą płaską zależy od kilku czynników:
1. Wielkość i kształt przedmiotu obrabianego
- Anoda płaska: Idealna do większych przedmiotów lub gdy wymagana jest równomierna grubość warstwy na większej powierzchni. Doskonała do galwanizacji w kąpieli.
- Anoda prętowa: Lepsza do mniejszych przedmiotów lub gdy powłoka ma być nanoszona tylko na określone obszary. Doskonała do galwanizacji tamponowej.
2. Rozkład prądu
- Anoda płaska: Zapewnia bardziej równomierny rozkład prądu, ponieważ posiada większą powierzchnię – idealna do równomiernych powłok.
- Anoda prętowa: Może powodować nierównomierne osadzanie, szczególnie jeśli odległość od katody nie jest stała. W galwanizacji w kąpieli może to prowadzić do zbyt wysokiej gęstości prądu anodowego.
3. Ułożenie elektrod
- Anoda płaska: Symetryczne ustawienie dwóch przeciwległych anod płaskich umożliwia równomierne osadzanie metalu.
- Anoda prętowa: Należy ją ustawić tak, aby odległość od przedmiotu obrabianego była możliwie stała, aby uniknąć różnic w grubości powłoki. Prąd płynie zawsze najkrótszą drogą!
4. Anoda prętowa do galwanizacji tamponowej
- Anoda prętowa jest stosowana głównie w galwanizacji tamponowej, ponieważ umożliwia precyzyjne nanoszenie powłok.
- Idealna do poprawek na małych obszarach lub do przedmiotów, których nie można całkowicie zanurzyć w kąpieli galwanicznej.
5. Anoda płaska do galwanizacji w kąpieli
- Anody płaskie są szczególnie korzystne w galwanizacji w kąpieli, ponieważ zapewniają równomierne osadzanie metalu na większych przedmiotach.
- W kąpieli galwanicznej przedmiot jest opływany z kilku stron, co zapewnia jednorodną warstwę.
- Dwie przeciwległe anody płaskie zapewniają symetryczny rozkład prądu i znacznie poprawiają jakość powłoki.
Wniosek
- Dla równomiernej grubości powłoki i większych przedmiotów → anoda płaska, szczególnie w galwanizacji w kąpieli.
- Dla mniejszych lub miejscowych powłok → anoda prętowa, szczególnie w galwanizacji tamponowej.
- Zawsze uwzględniaj właściwości elektrolitu i rozkład prądu!
- Czego potrzebuję do galwanizacji?
-
1. Źródło prądu
- Regulowane źródło prądu stałego (zasilacz) z odpowiednim napięciem i natężeniem dla danego elektrolitu.
2. Roztwór elektrolitu
- Specjalny roztwór elektrolitu zawierający jony metalu (np. elektrolit miedziowy do osadzania miedzi, elektrolit niklowy do powłok niklowych).
3. Anoda (biegun dodatni, +)
- Anoda miedziana do powłok miedzianych
- Anoda niklowa do powłok niklowych
- Anoda cynkowa do elektrolitu cynkowego
- Anoda aluminiowa do elektrolitu chromowego (alternatywnie anoda platynowa)
- Anoda ze stali nierdzewnej lub platynowa do metali szlachetnych lub wybranych elektrolitów specjalnych
4. Katoda (biegun ujemny, -)
- Element/wyrob przeznaczony do powlekania (np. części metalowe, biżuteria).
5. Pojemnik
- Wanna lub pojemnik z tworzywa sztucznego (odporny chemicznie) do kąpieli galwanicznej.
6. Przewody i zaciski
- Krokodylki i przewody do połączenia elektrod ze źródłem prądu.
7. Środki do obróbki wstępnej i końcowej
- Środki czyszczące i aktywatory (np. odtłuszczacz, roztwory trawiące – w tym Kondycjoner).
- Pasywatory i środki ochronne (np. olej do brunirowania) w celu zabezpieczenia powłoki.
8. Środki ochrony indywidualnej
- Rękawice, okulary ochronne i ewentualnie ochrona dróg oddechowych – dla bezpiecznej pracy z chemikaliami.
- Jaki zestaw lub zasilacz powinienem wybrać?
-
Najpierw należy zdecydować, co chce się osiągnąć, czyli jaką warstwę chce się ostatecznie uzyskać.
Opcje to: chrom, miedź, nikiel i cynk.
Dodatkowo dostępne są kombinacje miedź/nikiel, chrom/nikiel oraz zestaw duży.
Zestaw do chromowania dostępny jest tylko w wersji chrom/nikiel, ponieważ przed chromowaniem zaleca się zawsze niklowanie, a warstwa chromu jest na nim nanoszona tylko cienko.
Miedź pod warstwą niklu jest często korzystna, ponieważ znacznie poprawia ochronę przed korozją, a także gdy chcemy wyrównać nierówności lub przed polerowaniem.
Duży zestaw jest bardzo dobrym wyborem, jeśli chce się wykonywać wszystkie rodzaje powłok.
Oczywiście każdy zestaw można później wykorzystać w inny sposób – wystarczy dokupić odpowiednie elektrolity i anody, aby nanieść inną warstwę.
Następnie pojawia się pytanie, jaki zasilacz będzie potrzebny. Mamy tutaj mały o maks. 3A oraz mocny o 10A.
Wybór zależy od tego, jak duży ma być przedmiot do powlekania. Jeśli w przyszłości planuje się powlekanie większych elementów, potrzebny będzie mocny zasilacz (10A). Wystarczy wtedy dokupić większe wanny do galwanizacji (oraz oczywiście elektrolity).
W galwanizacji pracuje się ogólnie z gęstością prądu, ponieważ każdy elektrolit ma swój optymalny zakres. Podaje się ją w A/dm².
Aby obliczyć potrzebny prąd, należy pomnożyć zalecaną gęstość prądu dla danego elektrolitu przez powierzchnię elementu w dm². Napięcie dostosowuje się automatycznie, gdy ustawi się odpowiednią wartość prądu za pomocą ograniczenia prądowego (napięcie zostanie automatycznie obniżone, aż do osiągnięcia wybranego prądu).
W tej tabeli można odczytać wymaganą wydajność w zależności od potrzeb.
Elektrolit Prąd wyjściowy 3A* 5A* 10A* Chrom 0,6 1 2 Miedź kwaśna 5 8,5 17 Miedź alkaliczna 15 25 50 Nikiel 10 17 34 Cynk 12 20 40 Cynk-Nikiel 3,3 5,5 11 * – maksymalna powierzchnia do powlekania w dm² przy najmniejszej możliwej gęstości prądu
- Czym jest galwanika?
-
Galwanizacja, znana także jako elektroplaterowanie, to proces elektrochemiczny, w którym na powierzchnię innego materiału nanoszona jest cienka warstwa metalu. Stosuje się go, aby uszlachetnić powierzchnię, zabezpieczyć przed korozją, zwiększyć odporność na zużycie lub poprawić wygląd.
Jak działa galwanizacja:
-
Przygotowanie przedmiotu: Element przeznaczony do powlekania musi zostać dokładnie oczyszczony z zanieczyszczeń, takich jak olej, tłuszcz czy rdza. To kluczowe dla dobrej przyczepności warstwy metalicznej.
-
Kąpiel elektrolityczna: Przedmiot zanurza się w kąpieli elektrolitycznej zawierającej jony metalu, który ma zostać osadzony. Powlekany element pełni rolę katody (ujemnie naładowanej), a anoda (dodatnio naładowana) stanowi źródło jonów metalu.
-
Przyłożenie prądu elektrycznego: Przez kąpiel przepuszcza się prąd stały. Dodatnio naładowane jony metalu przemieszczają się do ujemnej katody, gdzie osadzają się jako zwarta warstwa metalu. Grubość i jakość powłoki zależą od natężenia prądu (gęstości prądu), składu elektrolitu oraz czasu procesu.
-
Zakończenie: Po zakończeniu osadzania element jest płukany, a w razie potrzeby polerowany, aby uzyskać pożądane wykończenie.
Zastosowania galwanizacji:
- Ochrona przed korozją: Metale takie jak cynk lub nikiel nanosi się na stal, aby zapobiec powstawaniu rdzy.
- Powłoki dekoracyjne: Metale szlachetne, np. złoto lub srebro, stosuje się na biżuterii i elementach dekoracyjnych, by poprawić ich wygląd.
- Ochrona przed zużyciem: Twardsze metale, jak chrom, nakłada się na narzędzia lub części maszyn, aby wydłużyć ich żywotność.
- Zastosowania elektroniczne: Cienkie warstwy metalu nanosi się na płytki drukowane lub styki elektryczne, aby poprawić przewodność.
Galwanizacja jest szeroko stosowana w przemyśle i rzemiośle i odgrywa ważną rolę w wielu procesach produkcyjnych.
-
- Procesy galwanotechniczne
-
W poniższej sekcji przedstawiono różne metody galwanotechniki, a także podstawowe narzędzia pracy potrzebne do każdej z nich. Zasadniczo wyróżnia się trzy metody galwaniczne: galwanizację w kąpieli, galwanizację stykową/tamponową oraz galwanizację bębnową.
Przegląd metod
Wyróżnia się 3 sposoby galwanicznego osadzania metali: galwanizację w kąpieli, galwanizację stykową (zwaną też tamponową) oraz galwanizację bębnową. Każda z tych metod ma swoje zalety i wady.
Metoda Zalety Wady Galwanizacja w kąpieli - Automatyczny przebieg procesu galwanizacji
- Możliwe uzyskanie grubości od kilku mikrometrów do kilku milimetrów
- Wymagany mocny zasilacz
- Niezbędne duże zbiorniki/wanienki
- Wysokie zużycie elektrolitu
- Mało praktyczna do galwanizacji drobnych elementów
Galwanizacja stykowa / tamponowa - Możliwość galwanizowania dużych powierzchni
- Wystarcza zasilacz o małej mocy – prąd płynie tylko w niewielkim punkcie kontaktu
- Niewielkie zużycie elektrolitu
- Osiągalne są jedynie małe grubości warstw, stąd ograniczona ochrona antykorozyjna
- Proces nie przebiega automatycznie
- Bardzo czasochłonna
- Męcząca w pracy
Galwanizacja bębnowa - Świetna do galwanizowania drobnych elementów
- Stosunkowo równomierna powłoka dzięki ciągłej rotacji
- Proces przebiega automatycznie
- Szybkie załadunki bębna
- Wymagany mocny zasilacz
- Niezbędne duże zbiorniki
- Wysokie zużycie elektrolitu
- Na detalach powstają drobne ślady uderzeń
- Konieczna pewna liczba sztuk lub odpowiedni rozmiar bębna, by zapewnić stały kontakt
Metoda galwanizacji w kąpieli
W galwanizacji w kąpieli zarówno obrabiany detal, jak i anoda zanurzone są w elektrolicie. Po przyłożeniu prądu następuje osadzanie metalu na powierzchni detalu.
To metoda często stosowana w przemyśle. Zazwyczaj elementy są chromowane, złocone lub niklowane w bardzo dużych wannach. Często używa się stelaży, na których zawiesza się części do powlekania. Aby zwiększyć dopuszczalną gęstość prądu i przyspieszyć osadzanie, warto wprowadzić ruch kąpieli: napowietrzanie, cyrkulację pompą lub ruch stelaża.
Zaletą jest prostota prowadzenia procesu i możliwość pracy przy dużych prądach, co umożliwia osadzanie grubych warstw. Wadą są duże ilości elektrolitu potrzebne do napełnienia wanien. Dlatego w warunkach hobbystycznych metoda ta najlepiej sprawdza się przy mniejszych elementach.
Wymagane wyposażenie podstawowe
Do galwanizacji w kąpieli potrzebne są: regulowane źródło prądu stałego, wanienka/zbiornik oraz przewody połączeniowe.
Źródłem prądu może być zasilacz laboratoryjny z wyświetlaniem napięcia (V) i prądu (A). Zbiornik powinien umożliwiać całkowite zanurzenie przedmiotu i być odporny na alkalia oraz kwasy; poza tworzywami sztucznymi dobrze sprawdza się szkło. Do podłączenia zasilania do anody i detalu służą przewody – by uniknąć pomyłek, używaj czerwonego przewodu dla bieguna (+) i czarnego dla bieguna (−).
Powierzchnia anody
Zasada ogólna: powierzchnia anody powinna możliwie odpowiadać powierzchni obrabianego detalu. Zbyt mała anoda może prowadzić do nierównomiernego osadzania.
Dzieje się tak, ponieważ prąd w elektrolicie nie rozkłada się równomiernie (tzw. rozproszenie) i wybiera najkrótszą drogę. Tam, gdzie odległość jest mniejsza, gęstość prądu rośnie i warstwa osadza się grubsza. Kształt i rozmieszczenie anod muszą więc sprzyjać równomiernemu rozkładowi prądu.
Większa anoda nie pogarsza wyniku, jednak w zależności od elektrolitu może dochodzić do silniejszej pasywacji przy niekorzystnej gęstości prądu anodowego (wydajności anodowej), co ogranicza przepływ prądu. W takim przypadku anodę należy wyczyścić.
Metoda galwanizacji stykowej / tamponowej
Do galwanizacji elementów zamontowanych na stałe lub o dużych gabarytach najlepiej nadaje się galwanizacja stykowa. Używa się prętowej anody (+) z końcówką z tamponem z tkaniny lub gąbką (dla uproszczenia: „tampon”). Tampon nasiąka elektrolitem. Przy podłączeniu detalu jako katody (−) prowadzi się tampon po powierzchni ruchem kolistym. W ten sposób powstaje przepływ prądu, a po kilku sekundach w miejscu kontaktu osadza się metal.
Ruch kolisty jest kluczowy, ponieważ na małym polu kontaktu płyną duże prądy. Zatrzymanie się w jednym miejscu może powodować matowienie i lokalne ściemnienie (przypalenia) – tym szybciej, im większy prąd. Wymagane jest więc nieco praktyki, którą łatwo zdobyć. Ruch tam i z powrotem jest mniej korzystny, bo krótkie zatrzymania przy wysokiej gęstości prądu sprzyjają przypaleniom.
Preferowanymi materiałami anod są materiały obojętne, np. platyna lub grafit (czasem również stal nierdzewna) albo metal zgodny z danym elektrolitem.
Wymagane wyposażenie podstawowe
Do galwanizacji stykowej/tamponowej potrzebne są: regulowany zasilacz z cyfrowym odczytem napięcia i prądu, anoda prętowa z uchwytem (pisak galwaniczny), zestaw przewodów oraz tampon lub gąbka. Anodę (uchwyt anody) podłącza się do bieguna (+) zasilacza. Następnie montuje się tampon/gąbkę – pisak jest gotowy do pracy. Detal, jak w innych metodach, podłącza się do bieguna (−).
Gąbka i tampon
Gąbki/tampony to końcówki chłonące elektrolit. To konieczne, aby w czasie procesu utrzymać elektrolit między anodą a detalem i dostarczać jony metalu. Idealne tampony mają bardzo wysoką chłonność i są wytrzymałe. Nie powinny być zbyt cienkie – punktowy nacisk może powodować izolację i przerwy w przewodzeniu. Niewskazane są też szwy na powierzchni, bo mogą rysować metal.
Zagęszczacz / środek żelujący
Zagęszczacz (środek żelujący) to specjalny dodatek zagęszczający. Dodaje się go do elektrolitu, aby zwiększyć lepkość. Istnieją preparaty przeznaczone do konkretnych elektrolitów – użycie przypadkowych środków zwykle unieczynnia kąpiel. Dzięki zagęszczeniu elektrolit nie kapie, praca jest czystsza i oszczędniejsza. Nie należy jednak zbyt mocno zagęszczać.
Aby zagęścić elektrolit, odmierz potrzebną ilość do naczynia i przy równomiernym mieszaniu dodawaj żelator do uzyskania oczekiwanej konsystencji. Postępuj powoli i ostrożnie. W przypadku proszków unikaj pylenia. Jeżeli przesadzisz z zagęszczeniem, rozrzedź, dolewając niezagęszczonego elektrolitu.
Metoda galwanizacji bębnowej
Do galwanizowania dużych ilości drobnych elementów najlepiej nadaje się galwanizacja bębnowa, zwłaszcza dla części, których trudno montować na stelażach. Zasadniczo proces odpowiada galwanizacji w kąpieli, lecz detale znajdują się luzem w wolno obracającym się bębnie. Kontakt elektryczny realizuje pręt kontaktowy w osi bębna, swobodnie poruszające się bijaki (przewody z przewodzącą końcówką) lub odpowiednie punkty kontaktowe w ściankach bębna; napęd zapewnia silnik z przekładnią. Równomierny ruch daje dość równą powłokę, choć występują różnice – niektóre części dłużej pozostają w kontakcie i otrzymują grubszą warstwę, inne cieńszą.
Zaletą jest szybkie załadowanie – elementy wsypuje się luzem. Wadą są drobne ślady uderzeń na detalach wskutek mieszania, więc metoda mniej nadaje się do powłok lustrzanych (dla śrub itp. nie ma to znaczenia). Konieczna jest też minimalna liczba sztuk, by zapewnić nieprzerwany kontakt.
Wymagane wyposażenie podstawowe
Potrzebny jest bęben galwaniczny. Podstawowe komponenty instalacji to bęben, silnik z przekładnią oraz mechanika napędu – razem tworzą urządzenie do galwanizacji bębnowej. Podobnie jak przy galwanizacji w kąpieli, wymagany jest odpowiednio mocny regulowany zasilacz oraz zestaw przewodów.
Napełnianie bębna
Zasada ogólna: bęben należy napełniać w ok. 40–50% objętości wsadu. Zapewnia to swobodę ruchu elementów i zapobiega zakleszczeniom czy blokadzie. W przeciwnym razie punkty kontaktu mogą być niekorzystne i powłoka wyjdzie nierównomierna. Należy też dopilnować, by elementy miały kontakt z prętem kontaktowym.
Wskazówka: Kulki są idealnym materiałem wsadowym – nie klinują się, swobodnie się poruszają i sprzyjają uzyskaniu równomiernej powłoki.
- Jak to wygląda z napięciem i gęstością prądu?
-
W galwanizacji napięcie i gęstość prądu odgrywają kluczową rolę w jakości powłoki. Oba parametry muszą być starannie ustawione, aby uzyskać równomierne i wysokiej jakości metalowe pokrycie.
1. Napięcie:
- Funkcja: Napięcie (mierzone w woltach) napędza przepływ prądu elektrycznego przez elektrolit, transportując jony metalu z anody do katody (przedmiotu), gdzie osadzają się one jako powłoka metalowa.
- Wpływ: Zbyt wysokie napięcie może powodować zbyt szybkie osadzanie jonów metalu, co prowadzi do powłok chropowatych, porowatych lub nawet proszkowych. Zbyt niskie napięcie może natomiast spowolnić proces, zmniejszając jego wydajność i powodując nierównomierne pokrycie.
- Zależność od odległości: Napięcie należy dostosować do odległości między anodą a katodą, ponieważ opór elektrolitu rośnie wraz z dystansem. Im większa odległość, tym wyższe napięcie jest potrzebne, aby osiągnąć odpowiednią gęstość prądu. Wartości napięcia podane na naszych elektrolitach są orientacyjne i dotyczą odległości około 10 cm. Przy innej odległości należy napięcie odpowiednio skorygować.
- Wartości maksymalne: Pamiętaj, że maksymalne wartości napięcia można osiągnąć głównie w idealnych warunkach, np. przy ruchu kąpieli (mieszanie lub pompowanie), co zapewnia równomierny przepływ elektrolitu wokół przedmiotu i zapobiega powstawaniu miejsc nadmiernego osadzania.
2. Gęstość prądu:
- Definicja: Gęstość prądu to wartość prądu przypadająca na powierzchnię elektrody, podawana w amperach na decymetr kwadratowy (A/dm²). Określa ona stosunek natężenia prądu do powierzchni elektrody i ma kluczowe znaczenie dla jakości osadzania metalu.
- Wpływ na katodę (przedmiot): Gęstość prądu katodowego ma bezpośredni wpływ na jakość powłoki. Każdy elektrolit ma optymalny zakres gęstości prądu, w którym uzyskuje się najlepsze rezultaty. Zbyt wysoka gęstość prądu może powodować chropowate, gruboziarniste warstwy, a zbyt niska – niepełne lub nierównomierne pokrycie.
- Wpływ na anodę: Gęstość prądu anodowego jest istotna dla stabilności elektrolitu. Idealnie, metal w anodzie (zwykle taki sam jak osadzany) powinien rozpuszczać się w takim tempie, w jakim jest osadzany na katodzie. Zapewnia to stałe stężenie jonów metalu w elektrolicie i wydłuża żywotność kąpieli.
- Dostosowanie przez temperaturę i ruch: Wyższe gęstości prądu można stosować, zwiększając temperaturę oraz wprowadzając ruch elektrolitu lub przedmiotu. Ułatwia to transport jonów i poprawia równomierność powłoki.
- Zależność od kształtu przedmiotu i anody: Gęstość prądu zmienia się w zależności od geometrii przedmiotu i anody. Ponieważ prąd płynie najkrótszą drogą, może to powodować nierównomierne pokrycie, zwłaszcza w narożnikach i przy złożonych kształtach. Dopasowanie kształtu anody do przedmiotu oraz użycie elektrod pomocniczych może temu zapobiec.
Wzajemne zależności między napięciem a gęstością prądu:
- Napięcie i gęstość prądu są ze sobą powiązane – wyższe napięcie zazwyczaj powoduje większą gęstość prądu, jeśli opory w układzie (np. opór elektrolitu, właściwości powierzchni) pozostają stałe.
- Dostosowanie napięcia jest często konieczne, aby uzyskać wymaganą gęstość prądu, ale wpływ na nią mają także stężenie elektrolitu i temperatura.
Podsumowanie:
- Napięcie napędza proces i wpływa na szybkość osadzania metalu. Musi być precyzyjnie dobrane, z uwzględnieniem odległości między anodą a katodą, aby zapewnić równomierną powłokę.
-
Gęstość prądu określa ilość metalu osadzanego na jednostkę powierzchni i wpływa na jakość oraz wygląd powłoki. Musi być utrzymywana w optymalnym zakresie, aby uzyskać wysoką jakość.
- Zarówno gęstość prądu katodowego, jak i anodowego jest istotna: pierwsza wpływa na jakość powłoki, druga – na stabilność elektrolitu. Regulacja temperatury i ruch kąpieli może umożliwić stosowanie wyższych gęstości prądu i poprawić stabilność procesu.
- Właściwości poszczególnych powłok
-
Każda z naniesionych warstw posiada określone właściwości, które ostatecznie pozytywnie wpływają na jakość końcowego efektu. Choć powlekanie miedzią w przypadku wielu materiałów nie jest bezwzględnie konieczne, to jednak prowadzi do uzyskania lepszego jakościowo rezultatu.
Miedź osadza się szybko i zapewnia wyjątkowo gładką powierzchnię. Jest także bardzo łatwa do polerowania, co znacząco obniża koszty polerowania. Nikiel zwiększa odporność całej powłoki na korozję. Przy późniejszym chromowaniu w dużym stopniu wpływa na połysk warstwy chromu.
Ostatnią warstwę stanowi cienko naniesiona powłoka o pożądanym efekcie dekoracyjnym lub technicznym.
- Ochrona antykorozyjna powłok
-
Dobry poziom ochrony przed korozją uzyskuje się dopiero dzięki odpowiednio grubej warstwie lub poprzez odpowiednią kombinację warstw. Cienka warstwa chromu na żelazie praktycznie nie zapewni ochrony, dlatego stosuje się co najmniej układ nikiel–chrom. Dodatkową zaletą warstwy niklu pod spodem jest to, że jako nikiel błyszczący wzmacnia połysk powłoki. Jeżeli chcemy poprawić odporność korozyjną także w atmosferze redukującej, stosuje się kombinację miedź–nikiel–chrom, ponieważ w takich warunkach miedź sprawdza się lepiej.
Ogólna zasada brzmi:
Odporność korozyjna silnie zależy od rodzaju osadzanego metalu. Istnieją też duże różnice między typami elektrolitów. Wiele z nich tworzy powłoki z mikroskopijnymi porami – w tych miejscach ochrona nie występuje. Do „zamknięcia” porów potrzebne są większe grubości warstw. Kombinacja kilku warstw wyraźnie poprawia ochronę: poszczególne powłoki się uzupełniają, a odporność na korozję rośnie niemal wykładniczo – zgodnie z zasadą „1+1=5”.
Przykłady ochrony przed korozją
Nikiel:
Czysta warstwa niklu zapewnia dobrą ochronę dopiero od ok. 25 µm, natomiast w układach nikiel–chrom lub miedź–nikiel–chrom odporność znacząco rośnie.
Cynk:
Dla cynku zaleca się grubość około 10 µm. Cynk wykazuje działanie anodowe (ochrona katodowa stali), dzięki czemu chroni także niepokryte miejsca z żelaza/stali (np. pory lub obszary uszkodzone mechanicznie).
Cynk–nikiel:
To połączenie dwóch ochronnych pierwiastków: aktywnego cynku i pasywnego niklu. Razem tworzą warstwę o podwyższonej odporności. Typowe grubości to 5–10 µm. Powłoki te są odporne na korozję do ok. 180 °C, dlatego świetnie nadają się do zabezpieczania elementów silników spalinowych.
Poniżej przykład chromowanej ramy z oczywiście niewystarczającą grubością powłoki lub nieprawidłowo wykonaną warstwą podkładową:

- Kolejność nakładania powłok
-
Powlekanie przedmiotu odbywa się zazwyczaj w kilku etapach, w których na powierzchnię elementu nanoszone są różne warstwy. Każda z tych warstw posiada istotne właściwości, które wpływają na uzyskanie profesjonalnego efektu.
W zależności od materiału i stanu powierzchni konieczne jest jej wstępne przygotowanie. Na przykład materiały wrażliwe na kwasy, takie jak cynk, przed powlekaniem kwaśnym elektrolitem miedziowym wymagają warstwy naniesionej z alkalicznego elektrolitu miedziowego. Aluminium poddaje się obróbce w aktywatorze do aluminium, a miedź wymaga cienkiej warstwy palladu przed bezprądowym nakładaniem powłoki niklowej.
Praktyczny układ kolejności warstw po przygotowaniu powierzchni:
- Miedź błyszcząca - dla dobrego wyrównania powierzchni
- Nikiel - jako warstwa barierowa przeciw dyfuzji
- Złoto, srebro lub chrom - jako warstwa końcowa
Ostatnia warstwa jest zazwyczaj nakładana cienko.
- Rozproszenie w galwanotechnice
-
W tej części omawiamy bardzo ważny aspekt – rozkład gęstości prądu i tzw. zdolność krycia (throwing power). Kształt anody powinien być dopasowany do geometrii powlekanego detalu. Samo zwiększenie prądu spowoduje, że miejsca bliższe anodzie staną się ciemne i matowe, ponieważ lokalna gęstość prądu będzie zbyt wysoka.
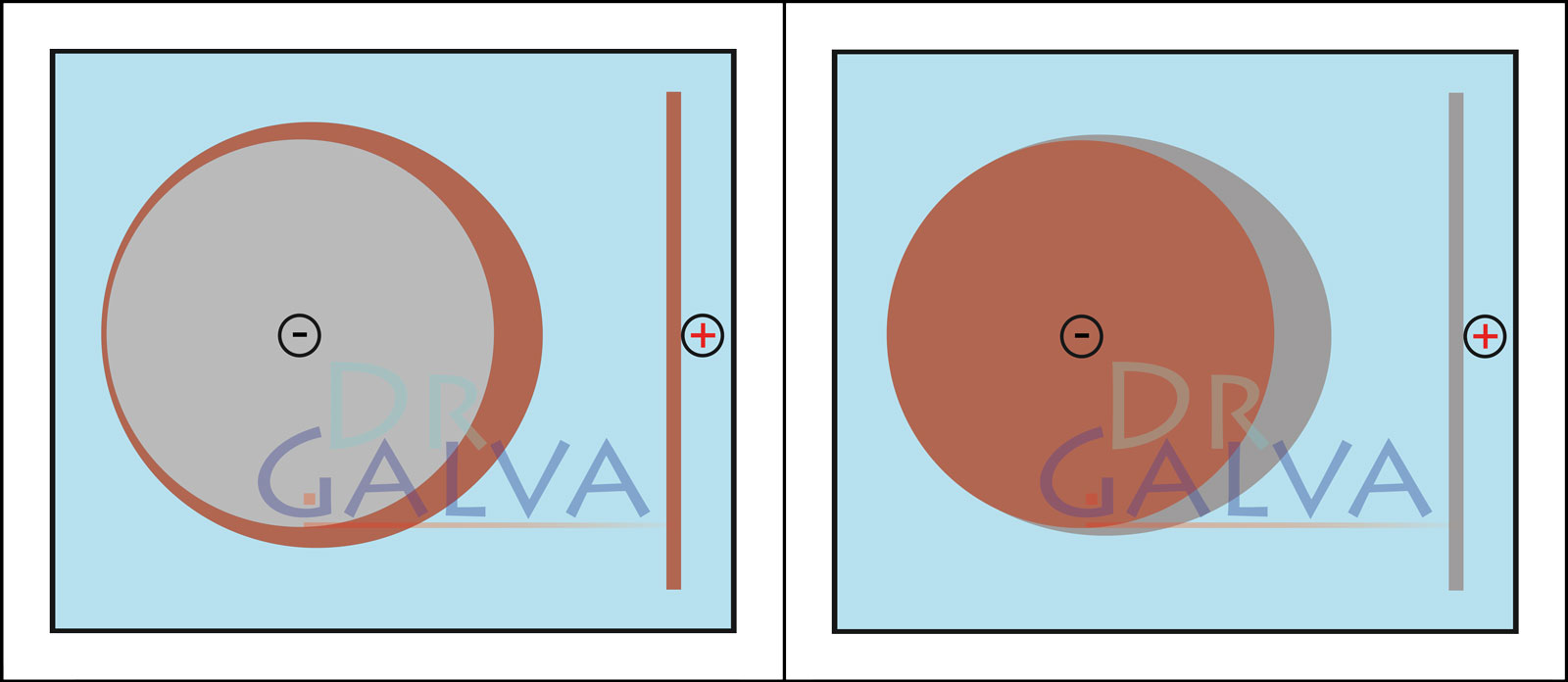
Dobra zdolność krycia (np. miedź kwaśna) przy zastosowaniu anody płaskiej. Im mniejsza odległość, tym większy przepływ prądu w tych miejscach i więcej metalu się tam osadza. Dzięki dobrej zdolności krycia również po stronie tylnej powstaje cienka warstwa. Słaba zdolność krycia (np. cynk słabo kwaśny). Metal osadza się tylko po stronie zwróconej ku anodzie. Po stronie tylnej praktycznie nie płynie prąd, więc nie następuje osadzanie, ewentualnie jedynie minimalne. 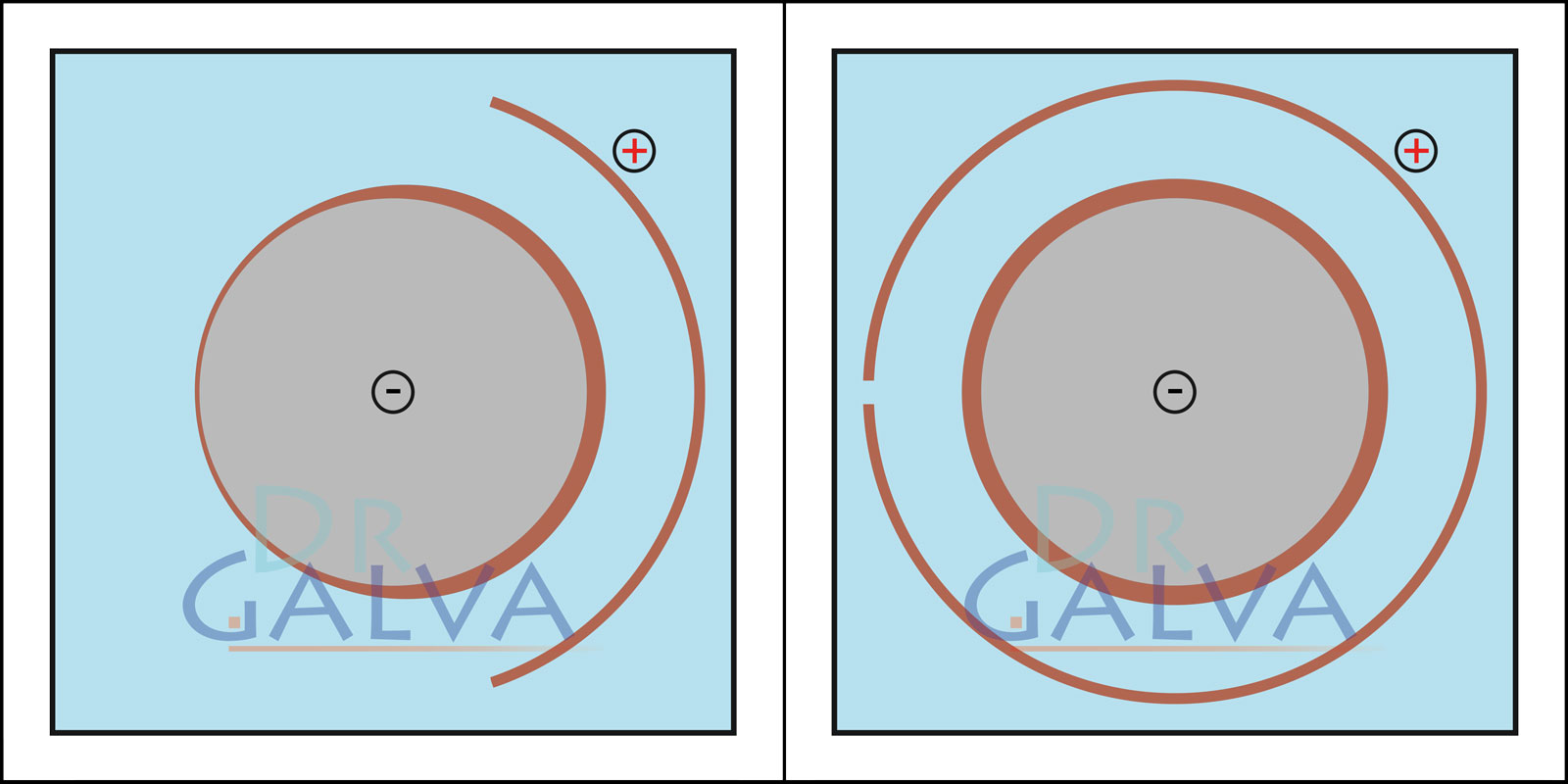
Przy anodzie dopasowanej do kształtu detalu metal osadza się znacznie równomierniej. Po stronie odwróconej od anody warstwa jest cieńsza, jednak całościowo rozkład grubości jest wyraźnie bardziej równy niż przy anodzie płaskiej. W kąpieli galwanicznej zastosowano anodę pierścieniową oraz detal. Dzięki temu odstęp anody od detalu jest jednakowy dookoła. Aby uzyskać równomierne osadzanie, nie ma potrzeby obracania detalu. 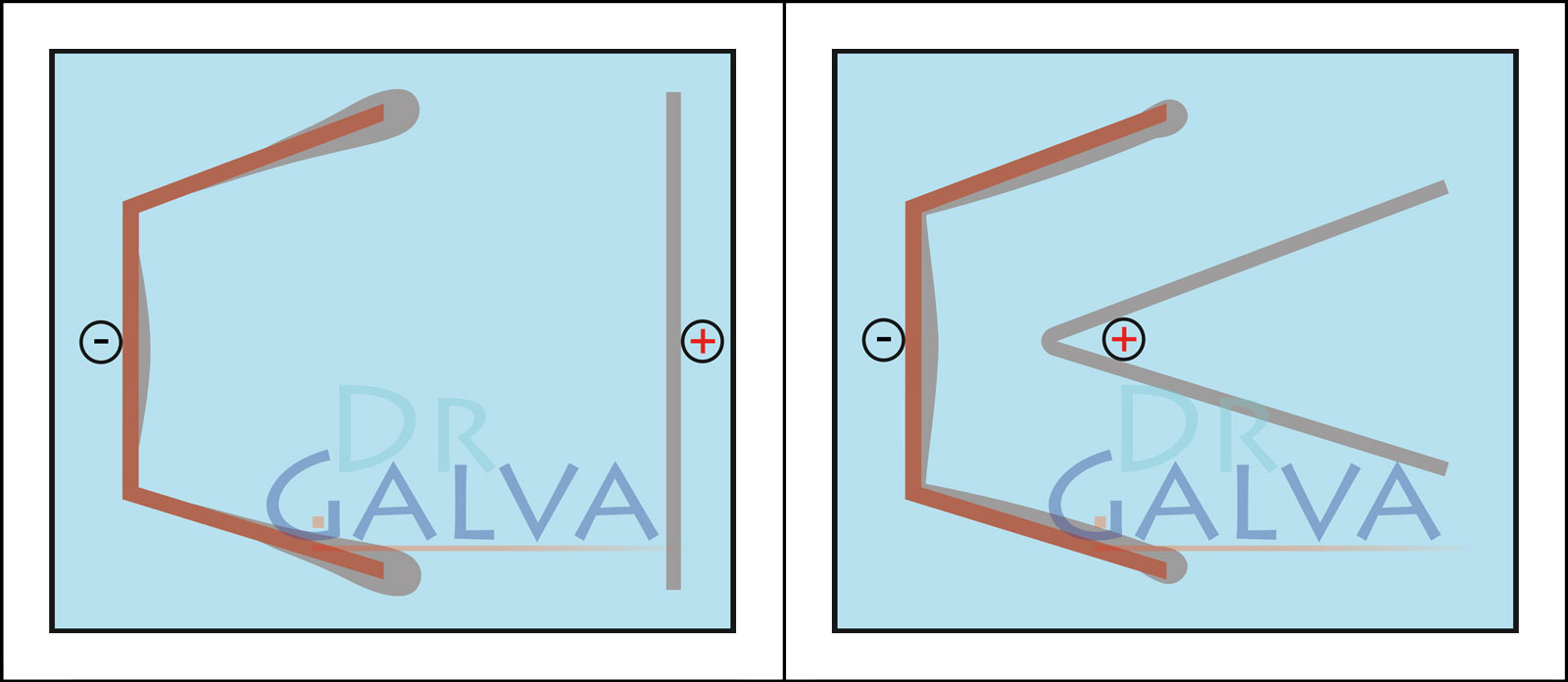
To najtrudniejszy przypadek – metal osadza się prawie wyłącznie w obszarze zwróconym ku anodzie. Z anodą dopasowaną do kształtu możliwe jest dobre osadzanie wewnątrz, a nawet pokrycie naroży. Jest to jednak rozwiązanie bardziej pracochłonne. - Dlaczego zawartość metalu jest stosunkowo mało istotna?
-
Zawartość jonów metalu (np. Cu²⁺, Ni²⁺, Zn²⁺) jest niewątpliwie ważnym parametrem sterującym elektrolitu do galwanizacji – ale to tylko jeden z wielu i w praktyce prawie nigdy nie jest czynnikiem ograniczającym jakość powłoki, ekonomikę ani stabilność procesu. Najważniejsze powody:
Dlaczego to nie jest “najważniejsze” Co (co najmniej) liczy się tak samo 1. Ograniczony wpływ powyżej minimum
Już przy umiarkowanych stężeniach dopływ jonów do katody jest nasycony. Wyższy poziom metalu daje tylko niewielki wzrost gęstości prądu, lecz zwiększa gęstość, lepkość i tworzenie szlamu.Gęstość prądu & rozkład
Ponad 90 % wad powłok (przypalenia, plamy, pory) zależy od lokalnej gęstości prądu – sterowanej geometrią, odstępem, mieszaniem i anodami pomocniczymi, a nie zawartością metalu.2. Strukturę krystaliczną determinują dodatki
Połysk, wielkość ziarna, naprężenia wewnętrzne i ciągliwość wynikają z poziomów ppm organicznych nośników (carrier), wybłyszczaczy (brightener) i wyrównywaczy (leveler) … całkowicie niezależnie od tego, czy w kąpieli jest 20 g L⁻¹ czy 30 g L⁻¹ Ni²⁺.Chemia dodatków & produkty rozkładu
Stosunek carrier/brightener zmienia osad znacznie silniej niż ±20 % Ni²⁺. Listy analityczne obejmują zwykle > 10 parametrów organicznych, ale tylko jeden parametr metaliczny.3. Przewodnictwo pochodzi głównie z matrycy soli
Straty omowe zależą przede wszystkim od jonów siarczanowych, chlorkowych lub fluoboranowych. Kąpiel srebra zawiera tylko 2–3 g L⁻¹ Ag⁺, a mimo to osiąga wysokie przewodnictwo dzięki 150 g L⁻¹ KCN.Jony przewodzące & pH
pH steruje wydzielaniem wodoru, połyskiem i naprężeniami; układy buforowe (kwas borowy, cytrynian) stabilizują elektrolit i powłokę.4. Termodynamika vs. kinetyka
Zawartość metalu prawie nie zmienia ΔG; kinetykę osadzania determinują temperatura, intensywność mieszania i kompleksowanie (EDTA, winian …).Temperatura & hydrodynamika
Wahanie o ±5 K często wpływa na rozkład grubości bardziej niż ±20 % metalu.5. Żywotność kąpieli & czynniki kosztowe
W kąpielach Cu i Ni koszty jonów metalu to < 20 % kosztu całkowitego na m² powłoki; wyższe są uzupełnianie dodatków, energia, czyszczenie, ścieki i analityka.Zarządzanie zanieczyszczeniami
Śladowy Cu w kąpielach Ni lub rozkład sacharynianu mogą zrujnować kąpiel, mimo że zawartość metalu jest “idealna”.6. Zawartość metalu nie definiuje “długości kampanii”
W elektrolitach samouzupełniających rozpuszczanie anody na bieżąco zastępuje metal osadzany na katodzie. “Czas pracy” kąpieli ogranicza więc degradacja dodatków, dopływ zanieczyszczeń i ubytek objętości – nie początkowa zawartość metalu.Materiał anody & mechanika rozpuszczania
Czystość anody, zawartość chlorków (w kąpielach Cu-OP) oraz właściwe okno gęstości prądu decydują o skuteczności redysolucji Cu, Ni, Zn itd. Dobrze prowadzona kąpiel utrzymuje poziom metalu przez miesiące, podczas gdy dodatki organiczne trzeba regularnie uzupełniać.Wniosek: Zawartość jonów metalu to jedynie fundament procesu galwanicznego. O jakości powłoki, stabilności i ekonomikę w większym stopniu decydują: zarządzanie gęstością prądu, dodatki, hydrodynamika, kontrola temperatury, rozpuszczanie anody i zanieczyszczenia.
- Anody rozpuszczalne - zalety, praktyka, ograniczenia
-
Anody rozpuszczalne składają się z metalu przeznaczonego do osadzania i ulegają rozpuszczaniu pod prądem. Dzięki temu uzupełniają jony metalu w elektrolicie proporcjonalnie do przepływu prądu – skład kąpieli pozostaje stabilniejszy bez ciągłego dodawania soli metali.
Zalety rozpuszczalnych anod
- Samo-uzupełnianie jonów metalu: rozpuszczanie anody ≈ osadzanie metalu → mniejszy nakład na uzupełnianie soli metali.
- Brak „dosalania” anionami: zamiast wprowadzać siarczany/chlorki przy każdej dolewce, do kąpieli trafia tylko metal → mniejsze zmiany przewodności i objętości, mniej korekt.
- Stabilniejsze warunki pH/redoks: utlenianie zachodzi poprzez rozpuszczanie metalu, a nie przez wodę/chlorek → mniej wydzielania O₂/Cl₂, mniejsza oksydacja dodatków.
- Niższe napięcie celi, lepsza efektywność energetyczna: rozpuszczanie metalu zwykle wymaga niższych potencjałów anodowych niż wydzielanie tlenu.
- Bardziej stała jakość powłoki: bardziej wyrównana aktywność metalu sprzyja równomiernemu połyskowi, drobnemu ziarnu i szybkości osadzania.
- Przyjazne w praktyce: mniej obsługi chemikaliów, rzadsze postoje dzięki większym, rzadszym dolewkom.
Typowa praktyka
- Nikiel: anody niklowe aktywowane siarką / granulki Ni w koszach Ti + odrobina chlorku, aby zapobiec pasywacji.
- Miedź (kwaśna): anody Cu z zawartością fosforu (fosforowane) + worki anodowe do zatrzymywania szlamu.
- Cyna, cynk i in.: powszechnie stosowane z anodami rozpuszczalnymi.
Ograniczenia / wady
- Szlam anodowy i pasywacja → wymagane worki anodowe, filtracja i odpowiednia gęstość prądu anodowego.
- Zanieczyszczenia metaliczne mogą współrozpuszczać się (istotna jakość anod).
-
Nie zawsze odpowiednie:
- Kąpiele Cr(VI) pracują z anodami nierozpuszczalnymi (bez przyrostu jonów metalu; pożądana inna elektrochemia).
- Kąpiele Cr(III): użycie anod z metalu chromu może wytwarzać Cr(VI) i uszkadzać elektrolit; dodatkowo Cr(III) jest zubażany przez osadzanie, co ogranicza żywotność kąpieli.
- Dlaczego Regenerator połysku, skoro anody już wzbogacają kąpiel?
-
W skrócie: Anody dostarczają (prawie wyłącznie) jonów metalu - połysk pochodzi z dodatków organicznych. Dodatki te nie powstają na anodzie i podczas pracy są stale zużywane lub rozkładane. Dlatego kąpiel wymaga regularnego nabłyszczacza uzupełniającego.
Dlaczego samo wzbogacanie przez anody nie wystarcza
- Anody rozpuszczają metal (np. Ni²⁺, Cu²⁺), utrzymując stałe stężenie metalu. Dodatki organiczne (carrier/suppressor, brightener/accelerator, leveler) pochodzą z zewnątrz - nie z anody.
- Zużycie na katodzie: Dodatki adsorbują się na powierzchni; część współosadza się lub ulega redukcji/rozkładowi elektrochemicznemu. Zależne od gęstości prądu i przepływu Ah.
- Rozkład na anodzie: Część składników organicznych ulega tam utlenieniu (zwłaszcza w kąpielach chlorkowych lub przy wysokiej polaryzacji anody).
- Straty uboczne: Wynos na detalach/uchwytach, adsorpcja w filtrze/worku anodowym, rozkład termiczny/chemiczny oraz oczyszczanie (np. węglem aktywnym) usuwają dodatki z kąpieli.
Rola nabłyszczacza uzupełniającego
- Zwykle zawiera krótkotrwałe, silnie aktywne składniki (często frakcję „akcelerator/nabłyszczacz”), które zużywają się najszybciej.
- Bez uzupełniania osad traci połysk, wyrównanie i drobne ziarno; mogą pojawić się matowe strefy, wyższe naprężenia lub chropowatość.
Wniosek
Anoda uzupełnia metal, nabłyszczacz uzupełniający uzupełnia funkcjonalne dodatki organiczne - oba są potrzebne do uzyskania równomiernych, błyszczących powłok.
Uwaga dotycząca trwałości kąpieli
Teoretycznie w elektrolitach regenerowalnych rozpuszczanie anod może pozwolić na nieograniczoną pracę, lecz inne dodatki są zużywane. Aby dalej używać drogiego elektrolitu, dodatki te się uzupełnia. Mimo to, bez specjalnych procesów oczyszczania elektrolit nie będzie działał bez końca - właściwa pielęgnacja dodatków może wielokrotnie wydłużyć jego żywotność.
- Jak zbudować ogniwo galwaniczne do osadzania metali?
-
Ogniwo galwaniczne do osadzania metali, zwane także ogniwem elektrolitycznym lub ogniwem do galwanizacji, to urządzenie służące do nanoszenia warstwy metalu na inny metal w procesie elektrochemicznym. Oto instrukcja krok po kroku, jak zbudować takie ogniwo:
Materiały:
- Źródło prądu: Regulowane źródło prądu stałego.
- Anoda: Na przykład anoda miedziana, jeśli ma być osadzana miedź. W przypadku niektórych roztworów należy użyć innej anody – sprawdź zalecenia dla danego elektrolitu.
- Katoda (przedmiot): Element metalowy, na którym ma zostać osadzony inny metal (np. biżuteria).
- Roztwór elektrolitu: Roztwór zawierający jony metalu, który ma zostać osadzony (np. elektrolit miedziany do osadzania miedzi).
- Pojemnik: Do utrzymywania roztworu elektrolitu.
- Przewody i krokodylki: Do podłączenia elektrod do źródła prądu.
Montaż:
-
Przygotowanie roztworu elektrolitu:
- Napełnij pojemnik roztworem elektrolitu. Do osadzania miedzi możesz użyć elektrolitu miedzianego.
- Napełnij pojemnik roztworem elektrolitu. Do osadzania miedzi możesz użyć elektrolitu miedzianego.
-
Umieszczenie elektrod:
-
Anoda: Umieść anody (np. płytki miedziane) w roztworze. Elektrody te dostarczą metalu do osadzania. Zaleca się użycie 2 przeciwległych anod dla równomierniejszego osadzania. Jeśli nie jest to możliwe, równomierną powłokę można uzyskać przez ciągłe obracanie przedmiotu.
Patrz także sekcja „Rozpraszanie w galwanizacji”. -
Katoda: Umieść katodę (np. biżuterię) w roztworze – to przedmiot, na którym będzie osadzany metal.
-
Anoda: Umieść anody (np. płytki miedziane) w roztworze. Elektrody te dostarczą metalu do osadzania. Zaleca się użycie 2 przeciwległych anod dla równomierniejszego osadzania. Jeśli nie jest to możliwe, równomierną powłokę można uzyskać przez ciągłe obracanie przedmiotu.
-
Podłączenie do źródła prądu:
- Podłącz anodę (płytkę miedzianą) do dodatniego bieguna źródła prądu.
- Podłącz katodę (przedmiot) do ujemnego bieguna źródła prądu. Katoda naładuje się ujemnie, co spowoduje osadzanie metalu na jej powierzchni.
-
Włączenie prądu:
- Włącz źródło prądu. Jony metalu w roztworze (np. jony Cu²⁺) będą przyciągane do katody, gdzie zostaną zredukowane do neutralnych atomów metalu i osadzą się na powierzchni.
Zasada działania:
- Anoda (płytka miedziana): Anoda częściowo się rozpuszcza pod wpływem przepływu prądu, uwalniając jony miedzi (Cu²⁺) do roztworu, co utrzymuje stałe stężenie jonów miedzi w elektrolicie:
Cu → Cu²⁺ + 2e⁻
- Katoda (przedmiot): Na katodzie jony Cu²⁺ z roztworu redukowane są przez elektrony do postaci metalicznej miedzi, która osadza się na przedmiocie:
Cu²⁺ + 2e⁻ → Cu
Ważne wskazówki:
- Natężenie prądu i czas: Określają grubość warstwy metalu. Większe natężenie i dłuższy czas dają grubszą warstwę.
- Temperatura: Temperatura roztworu może wpływać na szybkość osadzania – wyższa temperatura może przyspieszyć proces, ale też wpłynąć na jakość powłoki.
- Czystość roztworu: Zanieczyszczenia mogą pogorszyć jakość powłoki.
Efekt:
Dzięki temu układowi na przedmiocie powstaje równomierna warstwa metalu. To podstawowa zasada galwanizacji, stosowana w wielu procesach przemysłowych w celu powlekania metali oraz ochrony i uszlachetniania powierzchni.
Ogólny schemat:
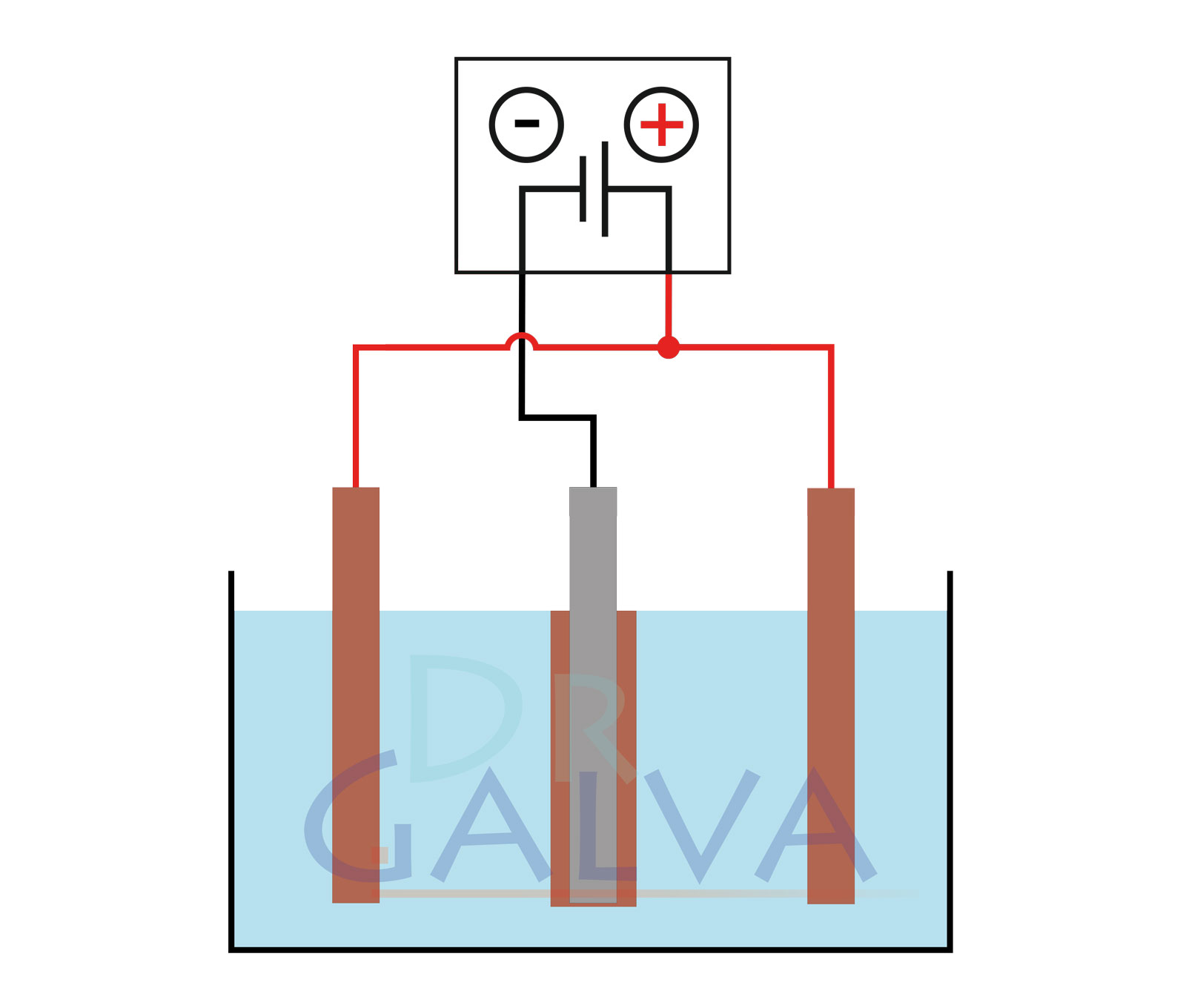
Porównanie osadzania:
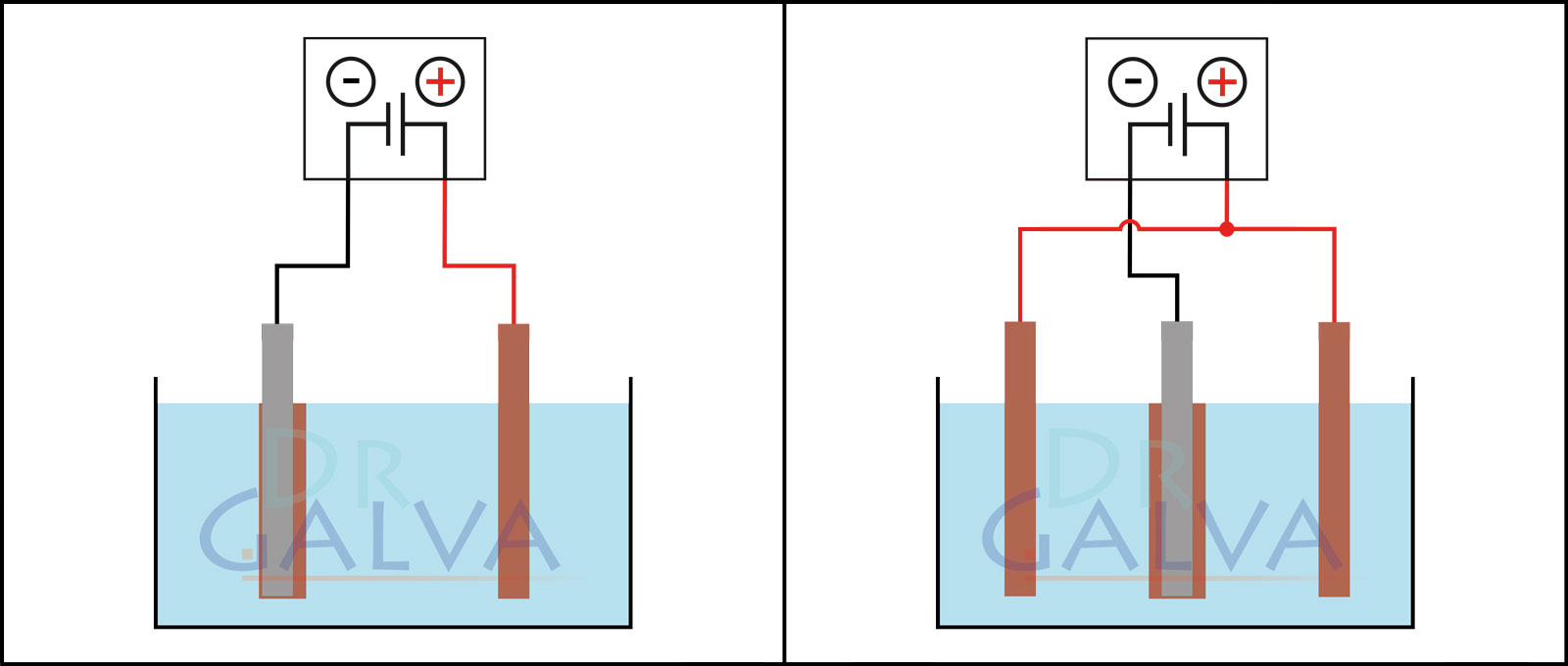
Anoda i przedmiot ustawione są naprzeciw siebie. Na przedniej stronie przedmiotu osadza się więcej metalu niż na tylnej. Przedmiot należy obracać w regularnych odstępach. Dwie anody i przedmiot znajdują się w zbiorniku. Obie anody powinny być podłączone do tego samego zasilacza. Przedmiot umieszczony jest centralnie między anodami, co zapewnia równomierniejsze osadzanie. - Prawidłowe odtłuszczanie powierzchni przeznaczonych do powlekania
-
Prawidłowe odtłuszczanie powierzchni przeznaczonych do powlekania jest kluczowym etapem procesu galwanizacji. Dokładne oczyszczenie jest niezbędne, aby zapewnić prawidłową przyczepność powłoki metalowej oraz wysoką jakość produktu końcowego. Oto najważniejsze kroki i metody skutecznego odtłuszczania:
Dlaczego odtłuszczanie jest ważne?
- Adhezja: Resztki tłuszczu i oleju mogą znacznie pogorszyć przyczepność powłoki galwanicznej.
- Jakość powłoki: Zanieczyszczenia prowadzą do nierównomiernych powłok, powstawania pęcherzyków i innych defektów.
- Ochrona przed korozją: Czyste powierzchnie zapewniają lepszą odporność korozyjną powlekanych materiałów.
Metody odtłuszczania
1. Odtłuszczanie chemiczne
- Czyszczenie rozpuszczalnikami: Stosowanie rozpuszczalników organicznych, takich jak aceton lub izopropanol, które skutecznie rozpuszczają tłuszcze i oleje.
- Aceton charakteryzuje się doskonałą rozpuszczalnością tłuszczów i niską temperaturą wrzenia. W laboratoriach jest głównie stosowany do czyszczenia lub odtłuszczania narzędzi roboczych. Dobrze usuwa odciski palców i lekkie tłuszcze, ale jest mniej skuteczny w przypadku olejów maszynowych. W rzeczywistości aceton może być niekorzystny przy elementach zabrudzonych olejem, ponieważ siły adhezji mogą powodować trwałe osadzanie się cząstek brudu na powierzchni.
- Izopropanol (propan-2-ol) ma szerokie zastosowanie i jest wyjątkowo uniwersalny. Może być używany do czyszczenia ekranów czy usuwania uciążliwych naklejek pozostawiających ślady kleju. Szczególnie dobrze sprawdza się tam, gdzie inne środki zawodzą, ponieważ całkowicie usuwa pozostałości. Odparowuje bez śladu i jest chemicznie neutralny wobec większości materiałów. Może być rozcieńczany wodą destylowaną i świetnie nadaje się do usuwania olejów oraz tłuszczów, a także do czyszczenia wielu powierzchni.
- Odtłuszczanie alkaliczne: Stosowanie środków alkalicznych w roztworach wodnych, które emulgują i usuwają tłuszcze oraz oleje.
- Kąpiele kwasowe: W niektórych przypadkach stosuje się środki kwaśne, szczególnie gdy trzeba usunąć tlenki metali lub rdzę.
2. Odtłuszczanie mechaniczne
- Szczotkowanie i szlifowanie: Użycie szczotek lub materiałów ściernych do usuwania grubych zanieczyszczeń.
- Piaskowanie/śrutowanie: Zastosowanie materiałów ściernych, takich jak mikrokulki szklane lub piasek, w celu dokładnego oczyszczenia powierzchni.
3. Odtłuszczanie elektrolityczne
- Odtłuszczanie anodowe: Przedmioty pełnią rolę anody w roztworze alkalicznym i są podłączone do prądu, co powoduje usuwanie tłuszczów i olejów dzięki wydzielaniu gazu.
- Odtłuszczanie katodowe: Przedmioty pełnią rolę katody, co często pozwala na delikatniejsze czyszczenie.
Kroki odtłuszczania
1. Przygotowanie
- Usunięcie grubych zanieczyszczeń i widocznego brudu przez spłukanie lub czyszczenie mechaniczne.
2. Odtłuszczanie chemiczne lub mechaniczne
- Zastosowanie wybranej metody odtłuszczania zgodnie z wymaganiami materiału i rodzaju zanieczyszczeń. W przypadku elementów zabrudzonych olejem należy użyć alternatywnych rozpuszczalników lub metod skuteczniejszych niż aceton.
3. Płukanie
- Dokładne płukanie elementów wodą destylowaną lub dejonizowaną, aby usunąć pozostałości środka odtłuszczającego.
4. Suszenie
- Starannie wysuszyć powierzchnię, aby uniknąć powstawania zacieków lub ponownego zabrudzenia.
Wskazówki dla najlepszego efektu
- Kontrola temperatury: Wiele procesów odtłuszczania jest skuteczniejszych w podwyższonej temperaturze.
- Kontrolowane środowisko: Praca w czystym otoczeniu zapobiega ponownemu zanieczyszczeniu.
- Kontrola jakości: Regularne sprawdzanie czystości powierzchni, np. test kropli wody lub pomiar kąta zwilżania.
Stosując te kroki i metody, zapewnisz optymalne przygotowanie powierzchni do powlekania, co przełoży się na wysoką jakość i trwałość powłoki galwanicznej.
- Jak używać elektrolitów galwanicznych?
-
Elektrolity stosuje się w postaci nierozcieńczonej, ponieważ są to roztwory gotowe do użycia. Parametry danego elektrolitu podane są na etykiecie butelki, podobnie jak informacja o wymaganej anodzie. Wartości napięcia mogą się różnić, ponieważ w roztworach obowiązuje prawo Ohma. Opór jest tutaj kluczowy i w zależności od odległości może powodować wzrost lub spadek przepływu prądu. Jeszcze dokładniejsze wyniki uzyskuje się, pracując w oparciu o gęstość prądu.
Elektrolity wzbogacają się również w trakcie rozpuszczania metalowej anody, co zwiększa ich wydajność (z wyjątkiem anod nierozpuszczalnych lub anod z metalu obcego).
Należy także pamiętać, że prąd zawsze płynie najkrótszą drogą.
- Ile można pokryć jednym elektrolitem galwanicznym?
-
Ilość materiału, jaką można osadzić za pomocą elektrolitu galwanicznego, zależy od kilku czynników:
Ważne czynniki wpływające
- Natężenie prądu i czas powlekania: Zgodnie z prawem Faradaya ilość osadzonego metalu jest bezpośrednio proporcjonalna do ładunku elektrycznego (prąd × czas).
- Skład elektrolitu: Zawartość jonów metalu w elektrolicie określa, jak długo można go używać, zanim konieczne będzie jego uzupełnienie lub regeneracja.
- Wydajność procesu: Sprawność osadzania różni się w zależności od metalu i elektrolitu (np. miedź i nikiel mają wyższą sprawność niż chrom).
- Grubość warstwy: Im grubsza warstwa, tym więcej materiału zostanie zużyte.
Przykład praktyczny
Jeden litr elektrolitu miedzianego o stężeniu 100 g/l miedzi może teoretycznie pokryć:
- 0,1 m² warstwą o grubości 100 µm lub
- 1 m² warstwą o grubości 10 µm.
Ważna uwaga
Rzeczywista powierzchnia, jaką można pokryć, jest często znacznie większa, jeśli stosuje się właściwe anody. Przy anodach rozpuszczalnych (np. niklowych lub miedzianych) osadzany metal jest stale uzupełniany, dzięki czemu elektrolit regeneruje się w trakcie procesu i może być używany znacznie dłużej.
- Czy elektrolity można ponownie wykorzystać?
-
Elektrolity można używać wielokrotnie. Należy jednak uważać, aby nie wprowadzać zanieczyszczeń, np. przez brud lub niewłaściwe anody. Może się także zdarzyć, że przedmiot ulegnie rozpuszczeniu w elektrolicie przy niewłaściwym doborze, np. stal ocynkowana w silnie kwaśnym elektrolicie.
- Czy anody można używać wielokrotnie?
-
Tak, anody stosowane w galwanizacji można używać wielokrotnie. Ponowne wykorzystanie anod jest opłacalne, o ile skutecznie dostarczają one jony metalu. Oto kilka ogólnych wskazówek:
-
Materiał anody: Anody często wykonane są z tego samego metalu, który ma być osadzany (np. nikiel, miedź, cynk). Podczas procesu galwanizacji ulegają one zużyciu, oddając jony metalu do kąpieli, które następnie osadzają się na przedmiocie (katodzie).
-
Zużycie anody: Z czasem anody częściowo rozpuszczają się w elektrolicie, ponieważ stanowią źródło jonów metalu w procesie powlekania. Tempo zużycia zależy od gęstości prądu, czasu galwanizacji oraz rodzaju elektrolitu.
-
Pielęgnacja i konserwacja: Anody należy regularnie kontrolować i w razie potrzeby czyścić, aby usuwać warstwy tlenków lub osady, które mogą obniżać ich wydajność. Odpowiednia konserwacja może wydłużyć żywotność anod.
-
Rodzaj procesu galwanicznego: W niektórych procesach konieczna jest częstsza wymiana anod niż w innych. Na przykład w procesie niklowania anody zużywają się wolniej niż w procesach o wyższej gęstości prądu lub specyficznych wymaganiach chemicznych.
- Wymiana anod: Jeśli anody są zbyt zużyte lub ich wydajność spada, należy je wymienić, aby zapewnić równomierną i wysokiej jakości powłokę.
Podsumowując, anody w galwanizacji można stosować wielokrotnie, o ile są w dobrym stanie i działają wydajnie. Regularna kontrola i konserwacja są kluczowe, aby maksymalnie wydłużyć ich żywotność.
-
Materiał anody: Anody często wykonane są z tego samego metalu, który ma być osadzany (np. nikiel, miedź, cynk). Podczas procesu galwanizacji ulegają one zużyciu, oddając jony metalu do kąpieli, które następnie osadzają się na przedmiocie (katodzie).
- Czy można stosować inne metale jako anody?
-
W galwanizacji kluczowe jest stosowanie wyłącznie anod specjalnie przeznaczonych do danego procesu. Inne materiały anod są niedozwolone, ponieważ mogą rozpuszczać się w elektrolicie i w ten sposób go zanieczyszczać. Takie zanieczyszczenie prowadzi do powstania powłoki o niższej jakości i może znacznie zakłócić cały proces galwanizacji. Dlatego ważne jest używanie zaleconych anod, aby zapewnić jakość i czystość powłoki galwanicznej.
- Czy można powlekać małe elementy za pomocą dużego zasilacza?
-
Tak, można powlekać małe przedmioty za pomocą dużego zasilacza, jednak ważne jest staranne regulowanie natężenia prądu. Mocny zasilacz może dostarczyć więcej prądu, niż jest potrzebne do małych obiektów, co może prowadzić do nadmiernego osadzania metalu, nierównych warstw, a nawet uszkodzenia elementu.
Zaleca się ustawienie prądu zgodnie z wymaganą gęstością prądu (prąd na jednostkę powierzchni) dla danego materiału i roztworu, aby uzyskać kontrolowaną i równomierną powłokę. Dobry zasilacz powinien umożliwiać precyzyjną regulację napięcia i natężenia, aby można było bezpiecznie i dokładnie powlekać także małe elementy.
- Czy mogę użyć baterii zamiast regulowanego zasilacza?
-
Choć teoretycznie możliwe jest użycie baterii zamiast regulowanego zasilacza do galwanizacji, stanowczo tego odradzamy. Powodem jest brak możliwości precyzyjnej regulacji napięcia i natężenia prądu, co jest niezbędne do pomyślnego przeprowadzenia procesu galwanizacji.
Dlaczego bateria jest nieodpowiednia:
-
Brak kontroli napięcia: Baterie dostarczają stałe napięcie (np. 1,5 V dla baterii AA lub 12 V dla akumulatora samochodowego). Ponieważ w galwanizacji napięcie często trzeba dostosowywać, aby kontrolować jakość powłoki, stałe napięcie z baterii często prowadzi do suboptymalnych rezultatów. Może to skutkować nierównymi warstwami, niekontrolowanym wydzielaniem gazów (np. powstawaniem pęcherzyków) i innymi niepożądanymi efektami.
-
Nieuregulowane natężenie prądu: Natężenie zależy od napięcia baterii i oporu kąpieli elektrolitycznej. Bez możliwości precyzyjnej regulacji może dojść do zbyt dużego przepływu prądu, który uszkodzi powłokę, lub zbyt małego, który uczyni proces nieefektywnym.
-
Spadek wydajności: W miarę użytkowania bateria traci wydajność, a napięcie spada. Bezpośrednio wpływa to na jakość i równomierność powłoki oraz może uczynić proces nieprzewidywalnym.
-
Ryzyko wadliwych powłok: Brak regulacji znacząco zwiększa ryzyko nieprawidłowych powłok, a nawet uszkodzenia elementu. Prowadzi to do niepotrzebnych strat materiału i dodatkowych kosztów.
Wniosek:
Aby uzyskać wysoką jakość i powtarzalność wyników galwanizacji, kluczowa jest precyzyjna kontrola napięcia i prądu. Bateria, która nie oferuje regulacji, nie spełnia tych wymagań i często daje niezadowalające efekty. Dlatego zalecamy użycie regulowanego zasilacza zaprojektowanego specjalnie do potrzeb galwanizacji, aby osiągnąć optymalne rezultaty.
-
- Czy można mieszać różne elektrolity?
-
Elektrolitów nie należy mieszać, ponieważ mogą być chemicznie i elektrochemicznie niekompatybilne. Szczególnie elektrolity zasadowe i kwasowe nie mogą być łączone – ich różne wartości pH prowadzą do niepożądanych reakcji, takich jak wytrącanie się metali lub innych substancji. W efekcie elektrolit staje się bezużyteczny, a powłoka wadliwa lub nierównomierna.
Mieszanie różnych elektrolitów metalicznych również nie działa. Na przykład elektrolitu miedziowego i cynkowego nie można po prostu połączyć, aby otrzymać mosiądz. Jony metali zachowują się w roztworze w odmienny sposób, przez co nie powstaje jednolita warstwa stopu.
Dodatki zawarte w każdym elektrolicie są precyzyjnie dopasowane do jego składu i wartości pH. Po zmieszaniu tracą swoje właściwości, a pożądane cechy elektrolitu zostają utracone.
- Po czym można rozpoznać, że elektrolit jest zużyty?
-
Wyczerpanie elektrolitu objawia się często spowolnieniem procesu osadzania lub zmianą koloru osadzonej warstwy metalu. Może również wystąpić blaknięcie pierwotnego zabarwienia elektrolitu lub zmniejszenie połysku powłoki.
Aby utrzymać stałą zawartość metalu, należy zawsze stosować odpowiednią anodę metalową. Podczas procesu anoda ta powoli się rozpuszcza i wzbogaca elektrolit w potrzebne jony metalu. Z biegiem czasu dochodzi jednak do zanieczyszczeń (obce jony, pozostałości organiczne, polimeryzacja), a środki nabłyszczające (jeśli występują) ulegają zużyciu.
W takim przypadku oferujemy środki odświeżające połysk, które uzupełniają brakujące środki nabłyszczające oraz inne dodatki.
W przypadku elektrolitów z anodami nierozpuszczalnymi (np. złoto) nie następuje automatyczne uzupełnianie metalu.
Elektrolit chromowy również można regenerować jedynie w bardzo pracochłonny sposób. Ponieważ chrom zazwyczaj jest nanoszony jedynie jako cienka warstwa wierzchnia na nikiel, odgrywa to jednak mniejszą rolę.
- Utylizacja roztworów
-
Zużyte roztwory można oddać do punktu zbiórki odpadów niebezpiecznych. Niewielkie ilości można zazwyczaj po rozcieńczeniu usunąć wraz ze ściekami.
Koniecznie zapoznaj się jednak z lokalnymi przepisami i wymaganiami.
- Gdzie znajdę kartę charakterystyki?
-
Znajdziesz to na stronie produktu w zakładce „Dokumenty”, gdzie możesz ją bezpośrednio pobrać/otworzyć.
- Czy tworzywa sztuczne można powlekać galwanicznie?
-
Tak, elementy z tworzyw sztucznych można powlekać galwanicznie. Początkowo powierzchnię tworzyw w tym celu trawiono kwasem chromosiarkowym, a następnie aktywowano palladem. Ponieważ jednak substancje te są bardzo toksyczne i szkodliwe dla środowiska, coraz częściej stosuje się bardziej przyjazną dla środowiska metodę: przewodzący lakier. Lakier przewodzący nadaje tworzywu właściwości przewodzące i eliminuje potrzebę używania szkodliwych chemikaliów. Proces ten jest więc znacznie bezpieczniejszy i bardziej zrównoważony.
Przebieg galwanicznego powlekania tworzyw sztucznych z użyciem lakieru przewodzącego:
- Przygotowanie powierzchni: Tworzywo jest dokładnie czyszczone w celu usunięcia tłuszczu, kurzu i innych zanieczyszczeń, które mogłyby pogorszyć przyczepność.
- Nakładanie lakieru przewodzącego: Specjalny lakier przewodzący zawierający cząsteczki metalu (np. miedzi lub srebra) jest równomiernie nanoszony na powierzchnię tworzywa. Lakier ten zapewnia przewodnictwo elektryczne i stanowi bazę dla procesu galwanicznego.
- Warstwa wstępna (np. miedź kwaśna): Powierzchnia pokryta lakierem przewodzącym jest galwanicznie powlekana cienką warstwą kwaśnej miedzi w celu uzyskania stabilnego, ciągłego przewodnictwa.
- Powlekanie galwaniczne: Następnie tworzywo można powlec wybraną warstwą metalu (np. niklem, a następnie chromem lub złotem). Grubość warstwy i wybór metalu zależą od konkretnych wymagań estetycznych i funkcjonalnych.
Zalety metody z lakierem przewodzącym:
- Przyjazna dla środowiska: Brak użycia kwasu chromosiarkowego i palladu, co znacznie zmniejsza obciążenie środowiska oraz ryzyko dla zdrowia.
- Uniwersalność: Lakier przewodzący można nanosić na wiele różnych rodzajów tworzyw, co umożliwia równomierne powlekanie.
- Wydajność: Bezpośrednie przejście od lakieru przewodzącego do powlekania galwanicznego pozwala na szybki i opłacalny proces.
Obszary zastosowania:
- Przemysł motoryzacyjny: Chromowane elementy z tworzyw sztucznych, takie jak listwy ozdobne i emblematy, wytwarzane bez użycia szkodliwych chemikaliów.
- Dobra konsumpcyjne i elektronika: Uszlachetnianie i funkcjonalizacja obudów z tworzyw oraz elementów dekoracyjnych.
Stosowanie lakierów przewodzących jako alternatywy dla kwasu chromosiarkowego i palladu jest zrównoważonym, nowoczesnym rozwiązaniem dla wielu zastosowań w galwanice tworzyw sztucznych.
- Galwaniczne powlekanie stali nierdzewnej
-
Stal nierdzewną można powlekać galwanicznie, jednak wymaga to specjalnego przygotowania wstępnego. Pasywna warstwa tlenku na stali nierdzewnej utrudnia przyczepność metalicznych powłok. Sprawdzoną metodą uzyskania trwałej powłoki jest zastosowanie Nickel-Strike jako warstwy aktywującej.
Instrukcja krok po kroku
1. Czyszczenie powierzchni
- Usunięcie tłuszczu, oleju lub zanieczyszczeń odpowiednim środkiem czyszczącym.
- Następnie dokładne spłukanie wodą dejonizowaną.
2. Nickel-Strike jako warstwa pośrednia
- Cienka warstwa niklu jest osadzana elektrochemicznie.
- Zapewnia to aktywną powierzchnię i zapobiega odspajaniu się powłoki.
- Po procesie Nickel-Strike element należy bezpośrednio przenieść do następnej kąpieli galwanicznej, bez płukania.
3. Nakładanie powłoki głównej
Po Nickel-Strike można nanieść pożądaną warstwę metalu:
- Nikiel – dla powłok dekoracyjnych lub odpornych na korozję.
- Miedź – jako warstwa pośrednia do dalszych powłok.
- Chrom – dla błyszczących i odpornych na ścieranie powierzchni (powinna być obecna szczelna warstwa niklu).
- Cynk lub cynk-nikiel – dla ochrony przed korozją.
Dlaczego Nickel-Strike jest konieczny?
- Stal nierdzewna posiada pasywną warstwę tlenku chromu, która uniemożliwia bezpośrednie osadzanie metalu.
- Nickel-Strike usuwa tę warstwę i zapewnia powierzchnię o dobrej przyczepności.
- Bez Nickel-Strike powłoka galwaniczna często nie utrzymuje się trwale na stali nierdzewnej.
- Jak powleka się aluminium?
-
Gdy niepowlekane aluminium ma kontakt z tlenem, rozpoczyna się proces utleniania. Proces ten jednak utrudnia nakładanie powłok. Dlatego elementy z aluminium zawsze wymagają wstępnej obróbki aktywatorem do aluminium. Usuwa on warstwę tlenku i jednocześnie w tym samym procesie tworzy na powierzchni materiału warstwę cynku. W ten sposób aktywator zapobiega kontaktowi z tlenem i chroni przed ponownym utlenianiem. Aby niezawodnie zapobiec późniejszemu tworzeniu się pęcherzy pod powłoką, oferujemy naszym klientom aktywator do aluminium o niskiej lepkości.
Jednak cynk nie jest odporny na kwasy. Dlatego w następnym etapie pracy należy nałożyć warstwę miedzi alkalicznej/zasadowej, a następnie warstwę miedzi kwaśnej. W ten sposób tworzy się stabilną podstawę dla ewentualnych kolejnych warstw.
W zależności od stopu aluminium konieczne jest w pierwszym kroku trawienie powierzchni przed nałożeniem warstwy cynku za pomocą aktywatora do aluminium. Nałożona warstwa cynku jest ponownie trawiona, a obróbka aktywatorem powtarzana po raz drugi. Robi się to dlatego, że warstwa cynku po trawieniu staje się stosunkowo chropowata, co pozwala lepiej zamknąć pory. Proces cynkowania w tym wydaniu jest niestety dość skomplikowany.
Aby pochromować lub pozłocić aluminium, należałoby zastosować następującą kolejność:
- Kondycjoner do trawienia
- Aktywator do aluminium w celu wytworzenia warstwy cynkowej
- Elektrolit miedzi alkalicznej, aby uzyskać warstwę miedzi chroniącą przed kwasem
- Elektrolit miedzi błyszczącej (kwaśny)
- Elektrolit niklowy (Free-Nickel) jako warstwa barierowa przeciw dyfuzji
- Elektrolit chromowy lub złoty jako warstwa końcowa
- Aktywator aluminium do powłok galwanicznych
-
Zasada działania
Zincat tworzy na aluminium cienką, dobrze przylegającą warstwę wymienną cynku, która zapobiega natychmiastowemu ponownemu utlenianiu Al i czyni powierzchnię przewodzącą/aktywną dla kolejnych warstw elektrolitycznych (np. miedź alkaliczna).
Zasada podstawowa (chemia)
W silnie zasadowym roztworze (NaOH/KOH) przypowierzchniowa matryca Al rozpuszcza się do aluminianu; jednocześnie z kompleksowanego Zn (np. Zn(OH)42−) osadza się cynk metaliczny na powierzchni → warstwa wymiany.
Standardowy łańcuch procesu (galwaniczny)
- Odtłuszczanie (alkaliczne), dokładnie spłukać.
- Trawienie alkaliczne (krótkie), spłukać.
- Deoksydacja/desmut (np. z kondycjonerem lub na bazie azotanów), spłukać.
- Zincat (typ. 30–90 s; utrzymywać krótko, inaczej krucha warstwa).
- Double-zincate dla trudnych stopów: chemicznie zdjąć/aktywować → zincat ponownie. (Pierwsza warstwa często nie jest przyczepna i daje się zetrzeć.)
- Krótka aktywacja (łagodnie kwaśna), bez suszenia przejść dalej do galwanizacji.
-
Strike galwaniczny przy małej gęstości prądu:
- Strike miedziowy cyjankowy (klasyczny, bardzo niezawodny; toksyczny/uciążliwy środowiskowo) lub
- Miedź alkaliczna
- Następnie warstwy główne: np. miedź błyszcząca do budowy, nikiel/chrom dekoracyjny itp.
Zależności stopowe
- Odlewy Al-Si (wysokie Si), Al-Mg, wysokowytrzymałe stopy Al: niemal zawsze double-zincate; ewentualnie dłuższa deoksydacja.
- Świeżo lane/śrutowane powierzchnie: starannie aktywować pory i wyspy krzemowe; dostosować czasy trawienia/deoksydacji.
Typowe wady i środki zaradcze
- Odspajanie/pęcherze: zbyt gruby/stary zincat, tlenki/brud, długie postoje/czasy suszenia → krótsze czasy zincatu, świeże kąpiele, szybki transfer mokre-na-mokre (≤ 1–2 min).
- Ciemnoszary: zincat wyczerpany, niewystarczająca aktywacja → odnowić zincat, zoptymalizować aktywację.
- Chropowatość/ataki krawędzi: zbyt agresywna/przedłużona chemia trawienia → skorygować czasy/receptury.
Prowadzenie kąpieli (zincat)
- Silnie zasadowa, zawiera kompleksy Zn; obciążenie aluminianem rośnie z czasem → aktywność spada.
- Działania: filtracja, częściowe odnowienia/dodawki, krótkie czasy kontaktu, stała temperatura/zasadowość.
Bezpieczeństwo/Środowisko
Zincat jest żrący → stosować ŚOI (rękawice, okulary, fartuch), unikać rozprysków. Prowadzić płukania alkaliczne/czyste; ścieki zawierające Zn/Al traktować zgodnie z przepisami. Strajki cyjankowe wymagają rygorystycznych zasad BHP i gospodarki ściekowej.
- Jak mogę pokryć galwanicznie wydruk 3D?
-
Galwaniczne pokrywanie obiektów drukowanych 3D to proces wieloetapowy, który wymaga specjalistycznego wyposażenia i materiałów. Poniżej przedstawiono podstawowe kroki galwanicznego powlekania elementu wydrukowanego w 3D:
1. Przygotowanie wydruku 3D
- Czyszczenie: Dokładnie oczyść element, aby usunąć kurz, oleje i inne zanieczyszczenia. Można użyć alkoholu izopropylowego (IPA) lub innego odpowiedniego środka czyszczącego.
- Wygładzanie: Jeśli to konieczne, wygładź powierzchnię wydruku, aby zapewnić równomierne osadzanie powłoki. Można to zrobić poprzez szlifowanie lub wygładzanie chemiczne.
2. Nałożenie warstwy przewodzącej
- Natryskowa farba przewodząca: Pokryj element farbą lub tuszem przewodzącym. Takie preparaty zawierają zwykle miedź, srebro lub grafit, aby nadać powierzchni przewodność.
- Przewodzące powłoki: Alternatywnie zanurz element w roztworze przewodzącym lub nanieś powłokę przewodzącą metodą natrysku.
3. Przygotowanie do galwanizacji
- Mocowanie anody i katody: Zamocuj wydrukowany element jako katodę w kąpieli galwanicznej. Anodę stanowi zwykle metal, który chcesz osadzić (np. miedź, nikiel). Zwróć uwagę na parametry używanego elektrolitu.
- Roztwór elektrolityczny: Upewnij się, że stosujesz właściwy elektrolit dla metalu, który ma być osadzany. Każdy metal wymaga dedykowanej kąpieli.
4. Proces galwaniczny
- Źródło prądu: Podłącz anodę i katodę do źródła prądu stałego. Przepływ prądu umożliwia transport jonów metalu z anody na powierzchnię elementu.
- Ustawienie parametrów: Dobierz odpowiednie wartości natężenia prądu i napięcia, aby uzyskać równomierną powłokę.
5. Obróbka końcowa
- Płukanie: Wyjmij element z kąpieli i dokładnie spłucz wodą, aby usunąć pozostałości elektrolitu.
- Polerowanie i zabezpieczenie: Wypoleruj powierzchnię do wymaganego połysku i w razie potrzeby zabezpiecz ją lakierem bezbarwnym lub inną powłoką ochronną.
Materiały i wyposażenie
- Farba przewodząca
- Kąpiel galwaniczna i odpowiedni elektrolit
- Anoda dobrana do danego elektrolitu
- Źródło prądu stałego
- Środki czyszczące i narzędzia do polerowania
Wskazówki bezpieczeństwa
- Środki ochrony indywidualnej: Noś odpowiednie rękawice, okulary ochronne oraz – w razie potrzeby – ochronę dróg oddechowych.
- Wentylacja: Zapewnij dobrą wentylację stanowiska pracy, aby zminimalizować narażenie na opary chemiczne.
Galwaniczne powlekanie może znacząco poprawić właściwości mechaniczne i estetyczne wydruków 3D. Stosując się do powyższych kroków, przygotujesz wysokiej jakości elementy z metaliczną powłoką.
- Jak można powlekać chrom?
-
Powierzchnia pokryta chromem nie zapewnia wystarczającej przyczepności dla nowych powłok. Dlatego istniejącą warstwę chromu należy usunąć. Do tego celu należy używać specjalnie opracowanych środków do usuwania chromu. Roztwory te są szczególnie bezpieczne w użyciu – na przykład specjalne dodatki zapobiegają powstawaniu wysoce toksycznego chromu sześciowartościowego.
Zazwyczaj pod starą warstwą chromu znajduje się warstwa niklu. Należy ją ponownie aktywować za pomocą specjalnie opracowanego aktywatora przeznaczonego do nowego powlekania. Aby zapobiec ponownemu tworzeniu się warstwy tlenkowej, element należy niezwłocznie po reaktywacji warstwy niklowej poddać nowemu procesowi powlekania.
Alternatywnie istnieje również tzw. Gold-Strike, który można nakładać bezpośrednio na chrom. Proces ten polega na tym, że warstwa tlenkowa jest redukowana, a jednocześnie osadzane jest złoto.
- Dlaczego nie stosuje się anody chromowej? I dlaczego anoda aluminiowa jest dopuszczalna?
-
Trójwartościowe elektrolity chromowe: wybór anod
W przypadku trójwartościowych elektrolitów chromowych panują inne warunki chemiczne i elektrochemiczne niż w klasycznych kąpielach chromowych sześciowartościowych. Dlatego anody muszą być dobrane w taki sposób, aby nie zakłócały składu kąpieli i nie powodowały powstawania substancji niebezpiecznych dla zdrowia.
Dlaczego nie stosuje się anody chromowej w elektrolitach trójwartościowych?
-
Zachowanie rozpuszczania chromu
W kąpielach trójwartościowych chrom występuje już w stanie utlenienia +III, który jest stosunkowo stabilny. Anoda chromowa mogłaby jednak prowadzić do niekontrolowanego utlenienia do chromu(VI):-
Chrom(VI) (sześciowartościowy) jest wysoce toksyczny i rakotwórczy. Nawet niewielkie ilości w kąpieli stanowią poważne zagrożenie dla zdrowia i środowiska.
-
Chrom(VI) (sześciowartościowy) jest wysoce toksyczny i rakotwórczy. Nawet niewielkie ilości w kąpieli stanowią poważne zagrożenie dla zdrowia i środowiska.
-
Stabilność kąpieli
Kąpiele trójwartościowe są specjalnie zaprojektowane tak, aby zawierały możliwie mało lub w ogóle nie zawierały Cr(VI). Anoda chromowa zaburzyłaby tę równowagę, ponieważ podczas utleniania elektrochemicznego może powstawać Cr(VI). Pogarsza to jakość osadzania i niesie poważne zagrożenia.
-
Praktyka: anody obojętne lub specjalne
- Anody platynowe lub irydowe są bardzo dobrymi anodami obojętnymi, ponieważ są wyjątkowo odporne na działanie elektrolitu i praktycznie nie oddają materiału. Są jednak kosztowne.
- Anody grafitowe są również często stosowane, lecz mogą oddawać drobne cząstki grafitu do kąpieli (erozja/ścieranie). Mogą one osadzać się na powierzchni elementu i powodować ciemne osady.
Dlaczego anoda aluminiowa jest dopuszczalna?
-
Ochronna warstwa tlenkowa (pasywacja)
Aluminium tworzy na swojej powierzchni zwartą warstwę tlenku glinu (Al₂O₃). Warstwa ta pasywuje metal i znacznie ogranicza rozpuszczanie jonów aluminium do kąpieli.
-
Niewielkie zakłócenie chemii kąpieli
Przy typowych wartościach napięcia i pH w trójwartościowych elektrolitach chromowych aluminium zachowuje się w dużej mierze pasywnie. Do elektrolitu przedostaje się tylko niewielka ilość jonów Al³⁺, co sprawia, że skład i pH kąpieli są praktycznie niezmienione.
-
Aluminium się rozpuszcza, ale nie osadza
Chociaż pewna ilość aluminium faktycznie przechodzi do kąpieli w postaci Al³⁺, to praktycznie nie osadza się ono jako warstwa metaliczna z roztworu wodnego.- Osadzanie aluminium z roztworów wodnych jest termodynamicznie bardzo trudne, ponieważ woda ulega redukcji znacznie łatwiej (wydzielanie wodoru).
- Dlatego na elementach nie powstaje niepożądana powłoka aluminiowa.
-
Dostępność i koszty
Aluminium jest tanie, łatwe w obróbce i – o ile pasywacja działa niezawodnie – praktycznym materiałem anodowym do kąpieli trójwartościowych chromowych.
Wniosek
- Anoda chromowa w kąpielach trójwartościowych prowadziłaby do niepożądanego powstawania Cr(VI), który jest wysoce niebezpieczny dla zdrowia.
- Anody aluminiowe są dopuszczalne dzięki ochronnej warstwie tlenkowej, ponieważ praktycznie nie zanieczyszczają elektrolitu i nie powodują powstawania toksycznych produktów ubocznych.
- Anody platynowe i irydowe uważane są za bardzo trwałe anody obojętne, lecz są kosztowne.
- Anody grafitowe są tańsze, ale mogą uwalniać cząstki grafitu, co może powodować ciemne osady.
-
Zachowanie rozpuszczania chromu
- Chromowanie galwaniczne - DIY deluxe: krok po kroku do perfekcyjnego wykończenia chromowanego!
-
Chromowanie galwaniczne to niezawodna metoda uzyskiwania unikalnych powierzchni chromowych. Dzięki temu poradnikowi DIY oferujemy prostą instrukcję krok po kroku, aby pomóc Ci uzyskać perfekcyjny efekt chromu. Skorzystaj z naszego doświadczenia i osiągnij imponujący rezultat!
Chromować można metale takie jak: stal, stal nierdzewna, brąz, żelazo, mosiądz, miedź i odlew ciśnieniowy cynku. Powierzchnia chromowa nakładana jest na grubą warstwę niklu. Jest to trwałe i solidne wykończenie, mało podatne na zużycie i zarysowania.
1. Wprowadzenie do chromowania galwanicznego
Jeśli interesuje Cię chromowanie galwaniczne, jesteś we właściwym miejscu! Chromowanie galwaniczne to proces, w którym cienka warstwa chromu jest nanoszona na metal. Proces ten jest szczególnie popularny, ponieważ zapewnia wysoką trwałość i odporność. Dodatkowo efekt chromu wygląda świetnie i nadaje każdemu elementowi wyjątkowy charakter. Jak to działa? Element zanurza się w kąpieli z elektrolitem chromowym i poddaje działaniu prądu. Dzięki temu chrom z elektrolitu osadza się na elemencie, tworząc warstwę chromu. Aby uzyskać perfekcyjny efekt, należy jednak pamiętać o kilku ważnych wskazówkach. Dokładne oczyszczenie elementu przed chromowaniem jest absolutnie niezbędne. Równie istotny jest dobór odpowiedniego natężenia prądu i czasu trwania procesu. Mając te podstawowe informacje, jesteś gotowy, aby zamienić swój element w błyszczącą ozdobę.
2. Najważniejsze narzędzia i materiały
Aby uzyskać perfekcyjne wykończenie chromowe, potrzebujesz odpowiednich narzędzi i materiałów. Najważniejsze z nich to: urządzenie do galwanizacji składające się ze źródła prądu, elektrolitu chromowego i anody. Potrzebny jest także odpowiedni element do chromowania – czysty i wolny od rdzy, brudu oraz tłuszczu. Do przygotowania powierzchni można użyć papieru ściernego, wełny stalowej lub szczotki drucianej. Dodatkowo niezbędne są okulary ochronne, rękawice i maska, aby chronić się przed oparami chemicznymi. Mając te narzędzia i materiały, jesteś gotowy do stworzenia własnego wykończenia chromowego.
3. Przygotowanie powierzchni do wykończenia chromowego
Przed rozpoczęciem chromowania niezwykle ważne jest dokładne przygotowanie powierzchni. Tylko czysta i gładka powierzchnia zapewni idealną przyczepność i pełny efekt chromu. Najpierw należy dokładnie oczyścić powierzchnię z kurzu, brudu i tłuszczu, używając specjalnego środka do czyszczenia metalu lub łagodnego detergentu. Następnie trzeba ją obrobić drobnym papierem ściernym lub szczotką drucianą, aby usunąć nierówności i ślady rdzy, uważając, by nie uszkodzić elementu. Na koniec należy ponownie dokładnie oczyścić i wysuszyć powierzchnię przed rozpoczęciem chromowania. Staranna obróbka to podstawa perfekcyjnego wykończenia.
4. Proces chromowania galwanicznego
W przypadku chromowania elementów metoda galwaniczna jest jedną z najlepszych opcji. Jest stosunkowo prosta i pozwala uzyskać doskonały efekt. Proces ten wymaga jednak kilku kluczowych kroków, aby powłoka była równomierna i trwała. Powierzchnię elementu należy dokładnie oczyścić, aby usunąć wszelkie zabrudzenia lub tłuszcz, które mogłyby wpłynąć na przyczepność chromu. Następnie element zanurza się w kąpieli z roztworem chromu, co powoduje osadzenie warstwy chromu na powierzchni. Ważne jest, aby element był w ruchu przez cały proces, co zapewnia równomierne pokrycie. Po nałożeniu warstwy chromu element należy dokładnie wypłukać i wysuszyć, aby uzyskać perfekcyjne wykończenie.
5. Obróbka końcowa dla idealnego efektu
Po zakończeniu procesu chromowania galwanicznego warto przeprowadzić staranną obróbkę końcową, aby uzyskać perfekcyjny efekt. Najpierw należy usunąć wszelkie zanieczyszczenia, takie jak odciski palców czy drobiny kurzu, za pomocą miękkiej ściereczki lub mikrofibry. Następnie warto wypolerować powierzchnię specjalnym środkiem do czyszczenia chromu, który usuwa pozostałości, a jednocześnie chroni powierzchnię przed korozją i utlenianiem. Na koniec można nałożyć wosk lub powłokę ochronną, aby zabezpieczyć powierzchnię przed zarysowaniami i uszkodzeniami. Dzięki temu chromowe wykończenie będzie trwałe i efektowne.
6. Wskazówki i triki dla profesjonalnego efektu
Aby osiągnąć profesjonalny efekt chromowania galwanicznego, należy przestrzegać kilku zasad. Ważne jest, aby wykonywać wszystkie kroki zgodnie z instrukcją, bez skracania procesu. Równie istotny jest dobór wysokiej jakości materiałów i solidnego źródła prądu. Dokładne oczyszczenie elementu to podstawa równomiernej powłoki. Powierzchnia elementu powinna być wolna od zarysowań i nierówności. Dobra przygotówka i staranna praca to klucz do sukcesu.
7. Podsumowanie: DIY deluxe – z odpowiednią wiedzą do perfekcyjnego chromu
Efekt końcowy mówi sam za siebie: Twój samodzielnie pochromowany element lśni nowym blaskiem i jest gotowy do użytku. Mając odpowiednią wiedzę i odrobinę cierpliwości, chromowanie galwaniczne nie jest problemem nawet dla hobbystów. Ważne jest przestrzeganie zasad bezpieczeństwa i dokładne wykonywanie poszczególnych kroków. Z odpowiednim sprzętem oraz kilkoma trikami możesz nadać swoim projektom eleganckie i trwałe wykończenie. Na co więc czekasz? Spróbuj i nadaj swoim elementom perfekcyjny chromowy wygląd!
- Elektrolit miedziowy alkaliczny/zasadowy – Zastosowania
-
Jeśli żelazo lub materiały wrażliwe na kwasy, takie jak ołów, cynk, miedź czy stal, mają zostać pokryte miedzią metodą galwaniczną, warto zastosować do przygotowania elektrolit miedziowy alkaliczny. Na przykład cynk, bez wstępnego użycia elektrolitu miedziowego alkalicznego, zostałby rozpuszczony w kwaśnym elektrolicie. Aby temu zapobiec, łagodny dla materiału elektrolit alkaliczny pokrywa materiały wrażliwe na kwasy pierwszą warstwą miedzi i przygotowuje je do końcowego pokrycia elektrolitem miedziowym kwaśnym o wysokim połysku.
Kolejnym pozytywnym efektem jest doskonała przyczepność warstwy uzyskanej dzięki elektrolitowi miedziowemu alkalicznemu oraz poprawiona odporność na korozję. Alkaliczny elektrolit miedziowy marki Dr. Galva charakteryzuje się szczególnie drobnoziarnistym osadem i jest plastyczny.
- Czym różni się elektrolit miedziowy alkaliczny od kwaśnego?
-
W galwanotechnice istnieją dwa główne typy elektrolitów miedziowych: alkaliczne i kwaśne. Różnią się one składem, wartością pH oraz właściwościami powłok miedzianych, które tworzą.
Różnice między elektrolitami miedziowymi alkalicznymi i kwaśnymi:
pH:
- Elektrolit miedziowy alkaliczny: Ma wysoką wartość pH (zasadowy), często oparty na solach takich jak cyjanek miedzi lub siarczan miedzi; dla stabilizacji zawiera środki kompleksujące.
- Elektrolit miedziowy kwaśny: Ma niską wartość pH (kwaśny) i zazwyczaj oparty jest na siarczanie miedzi oraz kwasie siarkowym.
Właściwości osadzania:
- Elektrolit miedziowy alkaliczny: Doskonale nadaje się do powlekania materiałów wrażliwych na kwasy, takich jak cynk czy żelazo. Zapewnia dobrą przyczepność do tych materiałów i tworzy warstwę często bardziej plastyczną (duktylną), która lepiej znosi odkształcenia bez pękania.
- Elektrolit miedziowy kwaśny: Umożliwia uzyskanie gładkich, dekoracyjnych powłok o błyszczącej powierzchni. Często stosowany jest do dużych, prostych elementów metalowych, zapewnia szybsze osadzanie i drobniejszą strukturę krystaliczną.
Zastosowanie i obszary użycia:
- Elektrolit miedziowy alkaliczny: Często używany do elementów o skomplikowanych kształtach oraz tam, gdzie ważna jest równomierność osadzania na różnych podłożach, dobra przyczepność i plastyczność powłoki. Stosowany m.in. w elektronice, przy płytkach drukowanych i do pokrywania miedzią elementów żelaznych.
- Elektrolit miedziowy kwaśny: Idealny w zastosowaniach wymagających błyszczącej, dekoracyjnej powierzchni. Często wykorzystywany do dekoracyjnych powłok na metalach, np. w jubilerstwie lub jako warstwa bazowa pod chromowanie.
- Chcę pokryć stal miedzią – wybrać elektrolit kwaśny czy alkaliczny?
-
Do pokrywania stalowych elementów miedzią należy wybrać elektrolit miedziowy alkaliczny. Przy użyciu elektrolitu miedziowego kwaśnego może dojść do osadzania miedzi bezprądowo na stali. Ta niekontrolowana reakcja chemiczna prowadzi do powstania gruboziarnistej warstwy miedzi o słabej przyczepności, co pogarsza jakość powłoki.
Elektrolit alkaliczny umożliwia kontrolowane, elektrolityczne osadzanie miedzi, co skutkuje równomierną i trwale przylegającą warstwą. Elektrolity alkaliczne niestety nie dają błyszczącej powierzchni, dlatego często po nich stosuje się dodatkowo elektrolit miedziowy kwaśny o wysokim połysku, aby uzyskać dekoracyjne, błyszczące wykończenie. Dlatego w przypadku elementów stalowych powszechnie stosuje się najpierw elektrolit miedziowy alkaliczny dla zapewnienia dobrej przyczepności, a następnie elektrolit miedziowy kwaśny dla uzyskania lśniącej powierzchni.
- Dlaczego elektrolit miedziowy kwaśny nadaje się tylko w ograniczonym stopniu do żelaza?
-
Miedź może osadzać się bezprądowo na żelazie ze względu na różnicę potencjałów elektrochemicznych, ponieważ miedź jest szlachetniejsza od żelaza. Podczas takiego osadzania bezprądowego żelazo ulega utlenieniu w kwaśnym roztworze, a jony miedzi redukują się i odkładają na powierzchni żelaza.
To osadzanie bezprądowe prowadzi jednak do słabej przyczepności miedzi, ponieważ tworzą się gruboziarniste kryształy miedzi, które osłabiają połączenie między miedzią a żelazem.
Aby złagodzić ten problem, można wprowadzić element do roztworu pod napięciem, co powoduje, że osadzanie miedzi zachodzi elektrochemicznie. Zastosowane napięcie umożliwia kontrolowany proces osadzania i poprawia przyczepność miedzi. W ten sposób można w dużym stopniu uniknąć problemów związanych z osadzaniem bezprądowym.
Innym sposobem na uniknięcie tego problemu jest nałożenie cienkiej warstwy miedzi przy użyciu elektrolitu miedziowego alkalicznego.
- Do czego służy powłoka typu Nickel Strike?
-
Nickel-Strike przygotowuje stale i stale nierdzewne do procesu galwanizacji. Znany jest także pod nazwą „nikiel uderzeniowy” i nadaje się zarówno do powlekania bezprądowego, jak i do wszystkich procesów galwanicznych.
Nickel-Strike trawi powierzchnię materiału i rozpuszcza ewentualnie obecny chrom. Podczas tego procesu tworzy się warstwa bazowa z niklu, która zapewnia lepszą przyczepność kolejnych powłok.
Istotnym zastosowaniem jest również wstępna obróbka już niklowanych powierzchni, które przez dłuższy czas były narażone na działanie powietrza. W takich przypadkach Nickel-Strike usuwa istniejącą warstwę tlenku, która mogłaby negatywnie wpłynąć na efekt końcowy.
- Jak powlekać zmatowiały/utleniony nikiel?
-
Zmatowiały lub utleniony nikiel był przez dłuższy czas narażony na kontakt z tlenem. Powoduje to powstanie tlenków, które można usunąć za pomocą naszego preparatu Nickel-Strike, jednocześnie tworząc nośną warstwę niklu. Następnie można wykonać żądaną powłokę.
Obróbka wstępna przy użyciu Nickel-Strike nie jest konieczna, jeśli warstwa niklu została nałożona bezpośrednio przed dalszym procesem powlekania. Nową warstwę niklu należy pokryć kolejną powłoką w ciągu godziny, ponieważ warstwa tlenku zaczyna się stopniowo tworzyć.
- Czy elektrolit niklowy Free-Nickel jest wolny od niklu?
-
Nie, elektrolit niklowy Free-Nickel nie jest wolny od niklu. Nazwa „Free-Nickel” odnosi się do tego, że elektrolit ten może być sprzedawany bez ograniczeń, ponieważ spełnia wymagania prawne dotyczące sprzedaży osobom prywatnym. Wiele tradycyjnych elektrolitów niklowych w UE podlega surowym ograniczeniom i nie może być sprzedawanych wysyłkowo.
Elektrolit Free-Nickel został jednak specjalnie opracowany tak, aby spełniał te wymagania, dzięki czemu można go kupić online bez ograniczeń. Należy jednak pamiętać, że wciąż jest to elektrolit niklowy, który osadza nikiel i zawiera ten metal.
- Jak niklować galwanicznie: Prosty poradnik DIY
-
Galwaniczne niklowanie to prosta i niedroga metoda, aby szybko i skutecznie zabezpieczyć elementy metalowe. W naszym poradniku DIY znajdziesz wszystko, co musisz wiedzieć, aby samodzielnie niklować swoje części metalowe. Dowiedz się, jak szybko i efektywnie chronić oraz ulepszać swoje projekty! Nic nie daje większej satysfakcji niż pomyślne ukończenie własnego projektu. Na co więc czekasz? Do dzieła!
1. Dlaczego niklowanie galwaniczne?
Jeśli zastanawiasz się, dlaczego niklowanie galwaniczne to dobry wybór, jest kilka powodów. Przede wszystkim proces ten zapewnia wysoką odporność na korozję, co oznacza, że niklowany przedmiot będzie trwalszy i mniej podatny na rdzę oraz podobne uszkodzenia. Dodatkowo nadaje przedmiotowi błyszczącą i równomierną powierzchnię, która nie tylko wygląda estetycznie, ale także poprawia przewodnictwo elektryczne. Niklowanie galwaniczne zwiększa też odporność na zużycie i ścieranie, co jest szczególnie przydatne, gdy element jest regularnie eksploatowany. Ogólnie rzecz biorąc, ta metoda oferuje wiele zalet, które czynią ją atrakcyjną opcją dla osób chcących chronić i ulepszać swoje przedmioty.
2. Czym jest galwanizacja i jak działa?
Galwanizacja to proces nanoszenia warstwy metalu na inne podłoże. Jest to powszechna metoda ochrony elementów metalowych lub nadania im dekoracyjnego wyglądu. Proces odbywa się poprzez elektrolizę, podczas której prąd elektryczny przepływa przez roztwór zawierający metal, który ma być naniesiony na powlekany przedmiot. Powlekany element nazywa się katodą, a metal do osadzenia – anodą. Gdy prąd przepływa przez roztwór, jony metalu uwalniają się z anody i osadzają na katodzie, tworząc trwałą powłokę. Grubość powłoki zależy od czasu trwania procesu. Galwanizacja może być stosowana do wielu materiałów, takich jak stal, miedź, mosiądz czy aluminium. To tania i prosta metoda ochrony i dekoracji.
3. Jakie narzędzia są potrzebne do projektu DIY?
Aby przeprowadzić galwaniczne niklowanie, potrzebujesz kilku specjalnych narzędzi, które pomogą Ci zakończyć projekt z powodzeniem. Przede wszystkim potrzebujesz źródła prądu, np. baterii lub zasilacza. Potrzebny jest też elektrolit niklowy, który naniesie nikiel na metal. Konieczna będzie anoda niklowa i materiał katodowy. Potrzebujesz także odpowiedniego środka czyszczącego do przygotowania metalu przed niklowaniem. Papier ścierny lub szczotka druciana mogą również pomóc w przygotowaniu powierzchni. Nie zapomnij o rękawicach ochronnych i okularach, aby chronić się przed urazami. Mając te narzędzia i trochę wprawy, możesz z powodzeniem samodzielnie niklować galwanicznie.
4. Instrukcja krok po kroku dotycząca galwanicznego niklowania
Do galwanicznego niklowania potrzebne są specjalne materiały i narzędzia. Najpierw należy dokładnie oczyścić i odtłuścić elementy, aby zapewnić dobrą przyczepność powłoki niklowej. Następnie przygotuj roztwór niklowy w odpowiednim pojemniku. Kolejnym krokiem jest podłączenie źródła prądu i zanurzenie powlekanych elementów jako katody w roztworze. Pręt anody powinien być również zanurzony, ale nie może stykać się z powlekanymi częściami. Podczas procesu należy kontrolować natężenie prądu i czas, aby uzyskać odpowiednią grubość powłoki niklowej. Po zakończeniu procesu części trzeba dokładnie spłukać i wysuszyć. Ważne jest przestrzeganie zasad bezpieczeństwa i noszenie odpowiednich środków ochrony, aby uniknąć urazów. Dzięki tej instrukcji krok po kroku możesz z powodzeniem samodzielnie niklować galwanicznie.
5. Wskazówki i triki, aby uzyskać najlepszy efekt
Aby uzyskać najlepszy efekt niklowania galwanicznego, warto zastosować kilka wskazówek i trików. Po pierwsze, upewnij się, że masz wszystkie potrzebne materiały i narzędzia, zanim zaczniesz. Dokładne przygotowanie jest kluczem do sukcesu. Zwróć uwagę, aby powierzchnia była dokładnie oczyszczona i odtłuszczona, co zapewni optymalną przyczepność powłoki. Równomierny dopływ prądu i odpowiedni czas kąpieli galwanicznej są również kluczowe dla idealnego efektu. Jeśli zastosujesz te rady, z pewnością osiągniesz świetny rezultat i wyniesiesz swoje projekty DIY na wyższy poziom.
6. Zastosowanie niklowania galwanicznego
Jeśli zastanawiasz się, do czego stosuje się niklowanie galwaniczne, odpowiedź jest prosta: to metoda pokrywania przedmiotów metalowych cienką warstwą niklu. Ta powłoka chroni metal przed korozją i nadaje mu błyszczące wykończenie. Niklowanie galwaniczne jest szeroko stosowane w przemyśle elektronicznym, motoryzacyjnym oraz jubilerskim. To niedroga metoda uszlachetniania przedmiotów metalowych i ochrony ich przed czynnikami zewnętrznymi. Dzięki naszemu poradnikowi DIY możesz łatwo przeprowadzić ten proces w domu i samodzielnie uszlachetnić swoje elementy metalowe.
7. Ważne rzeczy, na które trzeba zwrócić uwagę przy niklowaniu galwanicznym
Jeśli zdecydowałeś się na niklowanie galwaniczne, pamiętaj o kilku istotnych kwestiach, aby osiągnąć najlepszy efekt. Przede wszystkim element musi być czysty, wolny od oleju, tłuszczu i innych zanieczyszczeń – dokładne czyszczenie odpowiednim środkiem jest niezbędne. Upewnij się, że natężenie prądu i czas procesu są dopasowane do materiału i wielkości elementu. Zbyt duże natężenie lub zbyt długi czas mogą dać niepożądany efekt. Pamiętaj też o zachowaniu wszystkich zasad bezpieczeństwa, aby uniknąć urazów lub uszkodzeń. Stosując się do tych wskazówek i nabierając wprawy, możesz uzyskać trwałą i atrakcyjną powłokę niklową.
8. Zalety i wady niklowania galwanicznego
Największą zaletą jest ochrona, jaką daje powłoka niklowa – zabezpiecza metal bazowy przed korozją i zużyciem. Ponadto poprawia wygląd przedmiotu, nadając mu błyszczące wykończenie. Wady to m.in. możliwy koszt (szczególnie przy zleceniu fachowcowi), trudność w uzyskaniu równomiernej warstwy oraz ryzyko alergii na nikiel w przypadku kontaktu ze skórą. Mimo to niklowanie galwaniczne jest popularną metodą ochrony i poprawy wyglądu elementów metalowych.
9. Jakie koszty może generować projekt DIY?
Do niklowania galwanicznego potrzebujesz źródła prądu (np. zasilacza), roztworu elektrolitu niklowego, anod, katod i przewodów, a także odzieży ochronnej. Koszty mogą się różnić w zależności od wielkości elementu i ilości materiału. Sprzęt można kupić lub wypożyczyć. Warto wcześniej ocenić, czy inwestycja się opłaci i czy planujesz korzystać z niego w przyszłości.
10. Podsumowanie: Niklowanie galwaniczne jako skuteczny sposób ochrony metalu
Galwaniczne niklowanie to skuteczna metoda ochrony metalu przed korozją i zużyciem. Cienka warstwa niklu nadaje powierzchni połysk i atrakcyjny wygląd. Co najlepsze, proces ten można łatwo wykonać samodzielnie w domu, posiadając podstawowe narzędzia i materiały. To umiejętność, którą warto opanować – zarówno dla hobbystów, jak i profesjonalistów.
- Czy nikiel można osadzać bezpośrednio na mosiądzu?
-
Tak. Nikiel można galwanicznie osadzać bezpośrednio na mosiądzu. Dla pewnego startu zaleca się krótki nickel strike (kwaśny, bogaty w chlorki) jako warstwę pośrednią; następnie buduje się warstwę z niklu.
Zalecana sekwencja procesu
- Odtłuszczanie, dokładne płukanie.
- Mikrotrawienie dla stopów Cu/Zn (bardzo krótkie), płukanie.
- Aktywacja kwaśna (kondycjoner), przejście „mokre-na-mokre”.
- Nickel strike, start przy małej gęstości prądu, 20–90 s.
- następnie nikiel.
Wskazówki
- Unikać odcynkowania: krótkie czasy trawienia/aktywacji; bez etapów suszenia.
- Parametry startowe: najpierw niska gęstość prądu, potem szybko do wartości zadanej; umiarkowana zawartość chlorków sprzyja adhezji.
- Przeciw żółtawemu przebijaniu: zapewnić wystarczającą całkowitą grubość Ni.
Typowe wady i środki zaradcze
- Pęcherze/odspajanie: zbyt długie trawienie, zabrudzona powierzchnia, za wysoki prąd startowy → skrócić czasy, ponownie aktywować, start od niskiej gęstość prądu.
- Ciemnoszary start/pasywacja: unikać przestojów, odnowić aktywację.
- Chropowatość: poprawić filtrację/jakość płukań, wyeliminować źródła cząstek.
- Czy po cynkowaniu trzeba pasywować?
-
Czy pasywacja po cynkowaniu jest konieczna, zależy od przeznaczenia elementu i stawianych mu wymagań.
Nie zawsze obowiązkowa
W wielu standardowych zastosowaniach sama warstwa cynku (np. uzyskana poprzez cynkowanie ogniowe lub galwaniczne) jest wystarczająca, aby zapewnić podstawową ochronę przed korozją. Zwłaszcza w przypadku elementów, które nie są narażone na szczególnie wysokie wymagania estetyczne lub odpornościowe, często rezygnuje się z pasywacji.
Zalety pasywacji
- Dodatkowa ochrona przed korozją: Pasywacje (np. chromatowanie w różnych kolorach, fosforanowanie itp.) tworzą dodatkową warstwę ochronną, która zabezpiecza cynk przed utlenianiem i wydłuża jego trwałość.
- Lepsza estetyka: Powierzchnie pasywowane mogą być wizualnie ulepszone w zależności od zastosowanej metody (np. niebieska, żółta, czarna itp.).
- Zmniejszenie ryzyka powstawania białej rdzy: Szczególnie na świeżo ocynkowanych powierzchniach może wystąpić tzw. „biała rdza”, gdy są one narażone na wilgoć lub kondensację. Pasywacja redukuje to ryzyko.
Specjalne wymagania
W przypadku elementów narażonych na ekstremalne warunki środowiskowe (np. mgła solna, wysoka wilgotność powietrza, agresywne chemikalia) lub wymagających określonego wyglądu (jak w przemyśle motoryzacyjnym czy w zastosowaniach dekoracyjnych), pasywacja lub chromatowanie jest zazwyczaj zalecane, a czasem wręcz wymagane.
Wniosek
Pasywacja po cynkowaniu nie jest w każdym przypadku obowiązkowa, ale daje wyraźne korzyści w zakresie ochrony przed korozją i estetyki. Jej konieczność zależy od warunków użytkowania oraz wymagań jakościowych.
- Chromianowanie na żółto – cynkowanie na żółto
-
Pod pojęciem chromianowania na żółto (potocznie nazywanego także „cynkowaniem na żółto”) rozumie się proces z zakresu galwanotechniki, w którym już ocynkowane powierzchnie są dodatkowo uszlachetniane poprzez żółtą pasywację. Efektem jest charakterystyczna żółtawa do złotej powierzchnia, która jest zarówno estetyczna, jak i odporna na korozję.
Jak działa chromianowanie na żółto?
-
Warstwa cynku jako podstawa
Najpierw metal (np. stal) jest cynkowany, czy to poprzez cynkowanie galwaniczne, czy ogniowe. Ta warstwa cynku stanowi bazę dla procesu chromianowania.
-
Obróbka chemiczna
Następnie przeprowadza się pasywację lub chromianowanie. W przypadku wariantu żółtego w procesie tym, dzięki specjalnemu roztworowi chromianowemu, powstaje typowy żółty do złotego odcień.- W przeszłości często stosowano chrom(VI), który obecnie jest w dużej mierze regulowany lub zakazany.
- Nowoczesne systemy coraz częściej bazują na chromie(III), aby spełnić wymogi środowiskowe i zdrowotne.
-
Powstawanie koloru
Powierzchnia cynku reaguje ze składnikami roztworu chromianowego, tworząc warstwę konwersyjną („warstwę chromianową”). Wzmacnia ona ochronę przed korozją i nadaje typowy żółto-złoty kolor.
Dlaczego chromianowanie na żółto?
- Poprawa estetyki: Żółto-złota powierzchnia jest dekoracyjna i poszukiwana w wielu branżach, np. w produkcji okuć, śrub czy elementów ozdobnych.
- Dodatkowa ochrona przed korozją: Warstwa chromianowa dodatkowo zabezpiecza cynk przed utlenianiem.
- Sprawdzony standard: Od dziesięcioleci elementy chromianowane na żółto uchodzą za wzór odporności korozyjnej połączonej z atrakcyjnym wyglądem.
Bez chromu(VI) vs. z chromem(VI)
- Zawierający chrom(VI): Starsze, powszechnie stosowane metody. Intensywnie żółte zabarwienie, jednak obecnie mocno regulowane lub zakazane ze względu na szkodliwy wpływ na środowisko i zdrowie.
- Bazujący na chromie(III): Znacznie bezpieczniejszy dla środowiska i zdrowia, kolor może być mniej intensywny, lecz technologia spełnia aktualne normy i stale się rozwija.
Zalety i ograniczenia chromianowania na żółto
Zalety
- Charakterystyczny żółto-złoty wygląd
- Dodatkowa ochrona korozyjna w porównaniu z samym cynkiem
- Szerokie zastosowanie, m.in. w motoryzacji, elektronice i gospodarstwie domowym
Wady
- Wymogi środowiskowe przy procesach z chromem(VI)
- Ograniczenie do odcieni żółtych/złotych
- Jakość silnie zależna od przygotowania i jakości warstwy cynku
Wniosek
Chromianowanie na żółto to obróbka wtórna ocynkowanych powierzchni, w wyniku której powstaje żółta lub złota warstwa chromianowa. Warstwa ta wzmacnia ochronę przed korozją i nadaje elementowi charakterystyczny żółto-złoty wygląd. Podczas gdy dawniej stosowano głównie roztwory zawierające chrom(VI), dziś coraz częściej używa się systemów opartych na chromie(III), aby sprostać wymaganiom środowiskowym i zdrowotnym. Mimo różnic w intensywności barwy i przebiegu procesu, powierzchnie chromianowane na żółto pozostają jedną z najpopularniejszych i najczęściej stosowanych metod w galwanice.
-
Warstwa cynku jako podstawa
- Chromianowanie na czarno - cynkowanie na czarno
-
Chromianowanie na czarno (potocznie nazywane także „czarnym cynkowaniem”) to proces z dziedziny galwanotechniki, w którym już ocynkowana powierzchnia jest poddawana specjalnej ciemnej pasywacji. Ta obróbka chemiczna tworzy głęboko czarną lub antracytową warstwę chromianową, która poprawia odporność korozyjną i nadaje wyrazisty ciemny wygląd.
Jak działa chromianowanie na czarno?
-
Warstwa cynku jako podstawa
Na początku metal (np. stal) jest cynkowany (galwanicznie lub ogniowo), aby zapewnić bazową ochronę cynkową.
-
Ciemna pasywacja
Po cynkowaniu następuje pasywacja/chromianowanie w specjalnym roztworze, którego skład powoduje czarne zabarwienie. Tradycyjnie stosowano w tym celu roztwory zawierające chrom(VI), które jednak ze względów zdrowotnych i środowiskowych są obecnie mocno ograniczone. Nowoczesne technologie oparte na chromie(III) lub całkowicie wolne od chromu(VI) są dziś powszechne i zapewniają bardzo ciemną powierzchnię.
-
Reakcja i tworzenie warstwy
W roztworze pasywującym istniejąca warstwa cynku reaguje z odpowiednimi substancjami chemicznymi. Powstaje warstwa konwersyjna (warstwa chromianowa), która barwi się na czarno i zapewnia dodatkową ochronę przed korozją.
Zalety i zastosowania
- Wyrazisty wygląd: Czarna powierzchnia jest ceniona z powodów estetycznych lub maskujących (np. w zastosowaniach wojskowych).
- Lepsza ochrona przed korozją: Warstwa chromianowa chroni cynk przed utlenianiem, wydłużając trwałość.
- Szerokie zastosowanie: Czarne chromianowanie stosuje się w przemyśle motoryzacyjnym, przy śrubach i elementach złącznych, w elektronice, w pracach hobbystycznych i w zastosowaniach dekoracyjnych.
Systemy na bazie chromu(VI) a wolne od chromu(VI)
- Procesy zawierające chrom(VI): Dawały intensywnie czarne zabarwienie, ale ze względów środowiskowych i zdrowotnych (np. zgodnie z rozporządzeniem REACH) są silnie ograniczone lub zabronione.
- Systemy wolne od chromu(VI)/na bazie chromu(III): Zapewniają ciemne zabarwienie, są bezpieczniejsze dla środowiska i zdrowia, a ich jakość w zakresie intensywności koloru i ochrony antykorozyjnej stale się poprawia.
Ograniczenia chromianowania na czarno
- Wrażliwość na intensywne użytkowanie: Obciążenia mechaniczne (np. tarcie, zarysowania) mogą powodować ścieranie się ciemnej warstwy chromianowej.
- Dokładność procesu: Aby uzyskać jednolicie czarny efekt, należy ściśle kontrolować parametry kąpieli i procesu (temperatura, czas, skład chemiczny).
- Zależność od jakości cynkowania: Dobre przygotowanie warstwy cynkowej jest kluczowe, ponieważ czarne zabarwienie dobrze się trzyma tylko na czystym i równomiernym cynku.
Wnioski
Chromianowanie na czarno, często określane jako „czarne cynkowanie”, to proces ciemnej pasywacji ocynkowanych powierzchni. Daje on głęboki czarny lub ciemny wygląd oraz dodatkowo zwiększa ochronę antykorozyjną. W wersjach wolnych od chromu(VI) jest to dziś bardziej przyjazna środowisku i zdrowiu metoda uzyskania atrakcyjnej, czarnej powierzchni.
-
Warstwa cynku jako podstawa
- Samodzielne cynkowanie galwaniczne: Przewodnik krok po kroku dla prostego projektu DIY!
-
Uwaga miłośnicy DIY: Samodzielne cynkowanie galwaniczne jest prostsze, niż myślisz! Dzięki naszemu przewodnikowi otrzymasz szczegółowy przegląd podstaw cynkowania i korzyści, jakie ono daje. Czas na ekscytujący projekt DIY!
1. Wprowadzenie
Hej, Ty! Chcesz nauczyć się, jak samodzielnie cynkować galwanicznie swoje metalowe części? Jesteś we właściwym miejscu! W tym poradniku pokażemy Ci krok po kroku, jak zrealizować swój projekt DIY. Zanim jednak zaczniemy, wyjaśnimy, czym właściwie jest cynkowanie galwaniczne. Jest to proces, w którym na metal nakłada się warstwę ochronną, aby zabezpieczyć go przed korozją. Warstwa ta składa się z cynku i jest nanoszona na metal w wyniku reakcji chemicznej. Teraz już wiesz, czego się spodziewać – zaczynajmy!
2. Czym jest cynkowanie galwaniczne?
Cynkowanie galwaniczne to proces, w którym na metal nakłada się warstwę cynku w celu ochrony przed korozją. Jest to jedna z najczęściej stosowanych metod zabezpieczania stali i żelaza przed rdzą. Proces odbywa się metodą elektrolizy – metal zanurza się w roztworze cynku, a przez element przepuszcza się prąd elektryczny. Powoduje to osadzanie się cynku z roztworu na metalu, tworząc warstwę ochronną. Cynkowanie galwaniczne jest niedrogą i skuteczną metodą ochrony metali i świetnie nadaje się do projektów DIY. Mając podstawową wiedzę i kilka narzędzi, możesz przeprowadzić cynkowanie galwaniczne we własnym domu.
3. Przygotowania
Zanim rozpoczniesz cynkowanie galwaniczne, musisz się dobrze przygotować. Upewnij się, że masz wszystkie potrzebne materiały i narzędzia, takie jak anoda cynkowa, kąpiel do cynkowania, źródło prądu i rękawice ochronne. Ważne jest też, aby przygotować odpowiednie stanowisko pracy – dobrze wentylowane i wolne od materiałów łatwopalnych. Przed cynkowaniem oczyść i odtłuść element, aby zapewnić optymalną przyczepność warstwy cynku. Pamiętaj o bezpieczeństwie – zawsze używaj rękawic i okularów ochronnych. Z takimi przygotowaniami możesz przystąpić do udanego projektu DIY.
4. Narzędzia i materiały do cynkowania
Aby przeprowadzić projekt cynkowania galwanicznego, potrzebujesz odpowiednich narzędzi i materiałów. Przede wszystkim wybierz odpowiedni elektrolit cynkowy, który możesz kupić u nas. Potrzebny będzie również odpowiedni pojemnik, w którym przygotujesz kąpiel i zanurzysz element – może to być np. pojemnik plastikowy lub garnek ze stali nierdzewnej. Niezbędny jest też prostownik do regulacji natężenia prądu, co zapewni równomierne cynkowanie. Potrzebujesz również anody cynkowej, którą zanurza się w kąpieli i która dostarcza cynku na powierzchnię elementu. Do oczyszczenia elementu przed cynkowaniem użyj papieru ściernego oraz środków czyszczących, np. izopropanolu.
5. Przygotowanie powierzchni
Przed rozpoczęciem cynkowania upewnij się, że powierzchnia elementu jest gładka i czysta. Usuń rdzę, a następnie delikatnie zmatow powierzchnię szczotką drucianą lub papierem ściernym, aby poprawić przyczepność warstwy cynku. Możesz także zabezpieczyć miejsca, których nie chcesz cynkować, odpowiednim smarem lub olejem, aby uniknąć nierównej warstwy. Używaj tylko preparatów przeznaczonych do cynkowania.
6. Przeprowadzenie cynkowania galwanicznego
Podłącz element (katodę) do prostownika i zanurz go w elektrolit cynkowy. Anoda cynkowa zostaje podłączona do dodatniego bieguna i oddaje jony cynku, które osadzają się na elemencie, tworząc powłokę ochronną. Im dłużej element pozostaje w kąpieli, tym grubsza będzie warstwa cynku. Po zakończeniu procesu dokładnie opłucz element w wodzie i wysusz.
7. Obróbka po cynkowaniu
Po zakończeniu cynkowania spłucz element wodą, usuń ewentualne resztki elektrolitu i wysusz. Dla dodatkowej ochrony możesz nałożyć warstwę wosku, oleju lub specjalnego preparatu antykorozyjnego, co poprawi wygląd i trwałość powłoki.
8. Błędy, których należy unikać
Najczęstsze błędy to niedokładne oczyszczenie powierzchni, użycie nieodpowiednich proporcji elektrolitu lub niewłaściwego natężenia prądu. Każdy z tych czynników może pogorszyć jakość powłoki. Staranna praca i przestrzeganie instrukcji są kluczem do sukcesu.
9. Podsumowanie
Samodzielne cynkowanie galwaniczne to opłacalny projekt DIY, który pozwala zaoszczędzić pieniądze i zdobyć nowe umiejętności. Wymaga trochę praktyki i cierpliwości, ale efekty mogą być naprawdę profesjonalne. Jeśli interesuje Cię obróbka metalu, warto spróbować tej techniki.
- Jak nakładać powłoki na cynk (również Zamak)?
-
Powloka galwaniczna na cynku lub odlewie ciśnieniowym cynku
Jeśli cynk (np. odlew ciśnieniowy cynku lub powierzchnie ocynkowane) jest już obecny jako podłoże i ma zostać nałożona dodatkowa powłoka galwaniczna (np. miedź, nikiel, chrom itp.), obowiązują nieco inne wymagania niż w przypadku stali. Cynk jest metalem stosunkowo reaktywnym i może być szybko atakowany przez silne kwasy lub zasady. Ma również tendencję do tworzenia tlenków, co może utrudniać dobrą przyczepność. Dlatego – szczególnie w przypadku odlewów ciśnieniowych cynku – zazwyczaj stosuje się tzw. „strike” (warstwę pośrednią) w celu zapewnienia niezawodnej przyczepności dla kolejnej warstwy wierzchniej. Jako warstwę pośrednią (strike) stosuje się alkaliczny elektrolit miedziowy.
Poniżej przedstawiono zalecaną kolejność procesu nakładania powłok galwanicznych na cynk lub odlew ciśnieniowy cynku:
-
Czyszczenie / Odtłuszczanie
Cel: Usunięcie tłuszczów, olejów i innych zanieczyszczeń.
Uwagi: Stosować odpowiednie (łagodne) środki czyszczące, ponieważ cynk może być atakowany w silnie zasadowym środowisku. Najczęściej stosuje się proces kąpieli zanurzeniowej, ewentualnie wspomagany ultradźwiękami lub myciem natryskowym. -
Płukanie
Cel: Usunięcie pozostałości środka czyszczącego, aby uniknąć zanieczyszczenia kolejnych kąpieli.
Wskazówka: Płukanie wieloetapowe (zimna lub ciepła woda) jest często zalecane w celu dokładnego oczyszczenia powierzchni. -
Lekkie trawienie / Aktywacja (Kondycjoner)
Cel: Usunięcie cienkich warstw tlenków i aktywacja powierzchni cynku.
Kondycjoner: Specjalna, lekko kwaśna kąpiel, lekko rozcieńczona (zgodnie z zaleceniami producenta), która delikatnie traktuje powierzchnię cynku, nie powodując jej nadmiernego ataku. -
Krótkie płukanie
Cel: Usunięcie pozostałości po trawieniu lub kondycjonerze, aby nie zanieczyścić kolejnych kąpieli.
-
Warstwa pośrednia (alkaliczny elektrolit miedziowy)
Cel: Nałożenie bardzo cienkiej, ale mocno przylegającej warstwy metalu jako bazy dla kolejnych powłok.
Alkaliczny elektrolit miedziowy:
- Zapewnia dobrą przyczepność do cynku, jeśli powierzchnia jest prawidłowo przygotowana.
- Jest bardziej przyjazny dla środowiska i bezpieczniejszy niż kąpiele zawierające cyjanki. -
Powłoka główna
Opcje:
- Dodatkowa warstwa miedzi (kwaśna) dla przewodności i wygładzenia.
- Nikiel dla ochrony przed korozją i twardości.
- Chrom (po niklu) dla połysku i odporności na zużycie.
- Inne metale lub stopy (np. mosiądz, cyna, brąz) w zależności od potrzeb. -
Płukanie / Obróbka końcowa
Cel: Usunięcie pozostałości elektrolitu i dodatków.
Opcjonalnie: Pasywacja lub uszczelnienie dla dodatkowej ochrony antykorozyjnej lub określonego wyglądu. -
Suszenie / Kontrola końcowa
Suszenie: Wirówka, piec z gorącym powietrzem lub podobne, aby zapobiec plamom wodnym.
Końcowe: Kontrola wzrokowa, pomiar grubości powłoki i testy przyczepności.
Skrót kroków procesu
- Odtłuszczanie / Czyszczenie
- Płukanie
- Lekkie trawienie / Aktywacja (Kondycjoner, rozcieńczony)
- Płukanie
- Warstwa pośrednia (Alkaliczny elektrolit miedziowy)
- Powłoka główna (np. miedź błyszcząca, nikiel)
- Płukanie / Obróbka końcowa
- Suszenie / Kontrola końcowa
-
- Zasilacz nic nie wyświetla lub nie osiąga napięcia
-
Zasilacze regulują przepływ prądu poprzez napięcie, co wynika z prawa Ohma. Jeśli nie jest podłączony żaden odbiornik, prąd nie może płynąć.
Jeśli ograniczenie prądu jest ustawione na zero, napięcie również spadnie do 0.
Ustawianie napięcia
- Przekręć pokrętła regulacji napięcia (grubej i precyzyjnej), aż na wyświetlaczu pojawi się żądane napięcie wyjściowe
- Upewnij się, że ustawione napięcie nie przekracza maksymalnego napięcia zasilania podłączonego odbiornika
- Jeśli nie można dalej zwiększyć napięcia, prawdopodobnie ograniczenie prądu jest ustawione zbyt nisko – zwiększ je
- Przepływ prądu wynika wtedy z oporu omowego
Ustawianie ograniczenia prądu
- Ustaw bardzo niskie napięcie, około 1 V, aby uniknąć iskrzenia, i wykonaj zwarcie z podłączonymi przewodami pomiarowymi
- Następnie zasilacz przełączy się z trybu stałego napięcia na tryb stałego prądu (na wyświetlaczu pojawi się C.C zamiast C.V)
- Przekręć pokrętła regulacji prądu (grubej i precyzyjnej), aż na wyświetlaczu pojawi się żądany prąd wyjściowy
- Po pomyślnym ustawieniu ograniczenia prądu można rozłączyć zwarcie
- Następnie zwiększ napięcie do żądanej wartości
- Jeśli pracujesz z ograniczeniem prądu, napięcie zostanie obniżone zgodnie z podłączonym oporem
Jeśli prąd nie płynie, należy sprawdzić podłączenie.
- Tworzy się czarny osad lub powłoka staje się matowa
-
Jeśli podczas galwanizacji pojawia się czarny osad lub powłoka staje się matowa, może to wskazywać na kilka problemów w procesie. Oto najczęstsze przyczyny:
Nadmierny prąd (prąd zbyt wysoki):
- Objaw: Tworzenie się czarnego osadu lub matowa, nierówna powierzchnia.
- Przyczyna: Zbyt wysoki prąd powoduje zbyt szybkie osadzanie się cząstek metalu, co prowadzi do powłoki o grubej strukturze, porowatej lub nawet czarnej. Jest to szczególnie częste, gdy gęstość prądu jest zbyt wysoka.
- Rozwiązanie: Zmniejsz prąd lub napięcie, aby uzyskać gładsze i bardziej równomierne osadzanie metalu (pamiętaj, że przy niektórych elektrolitach zbyt niska gęstość prądu również może powodować matowość).
Niewystarczające czyszczenie elementu:
- Objaw: Nierówna, matowa powłoka lub czarne plamy.
- Przyczyna: Zanieczyszczenia, tlenki lub tłuszcz na powierzchni zakłócają proces osadzania metalu.
- Rozwiązanie: Dokładnie oczyść element przed zanurzeniem w kąpieli elektrolitycznej – usuń tłuszcz, tlenki i brud poprzez mycie, szlifowanie i płukanie.
Nieodpowiedni materiał elementu:
- Objaw: Czarny osad w elektrolicie lub matowa powłoka.
- Przyczyna: Niektóre materiały mogą reagować z elektrolitem, zanieczyszczając kąpiel i pogarszając jakość powłoki.
- Rozwiązanie: Upewnij się, że materiał jest kompatybilny z elektrolitem – wybierz odpowiednią kąpiel, aby uniknąć reakcji chemicznych powodujących zanieczyszczenie.
Niewłaściwe ustawienie elektrod:
- Objaw: Czarne osady w określonych miejscach.
- Przyczyna: Nierówny rozkład prądu przez złe rozmieszczenie anody lub katody.
- Rozwiązanie: Ustaw elektrody tak, aby prąd był rozłożony równomiernie; sprawdź odległości między elektrodami a elementem.
Zbyt długi czas galwanizacji:
- Objaw: Matowa lub ciemna powłoka.
- Przyczyna: Nadmierne nasycenie osadzanej warstwy może powodować zmianę koloru i strukturę powierzchni.
- Rozwiązanie: Skróć czas galwanizacji i monitoruj proces, aby osiągnąć żądaną grubość powłoki bez pogorszenia wyglądu.
Zbyt wysoka lub niska temperatura elektrolitu:
- Objaw: Matowość lub czarne osady.
- Przyczyna: Odchylenia temperatury zmieniają szybkość reakcji chemicznych w kąpieli, pogarszając jakość powłoki.
- Rozwiązanie: Kontroluj temperaturę kąpieli, aby była w optymalnym zakresie dla danego procesu.
Podsumowanie:
Czarny osad lub matowa powłoka przy galwanizacji najczęściej wynikają z nadmiernego prądu, złego czyszczenia, nieodpowiedniego materiału, nierównomiernego rozkładu prądu lub problemów z temperaturą. Korekta tych parametrów znacznie poprawi jakość powłoki.
- Osadzanie chromu staje się ciemne
-
To normalne, że chrom w początkowych fazach osadzania wydaje się ciemny. Wynika to z faktu, że warstwa chromu jest początkowo bardzo drobnokrystaliczna, co powoduje inne odbijanie światła i sprawia, że powierzchnia wygląda na ciemną. W miarę postępu procesu kryształy się powiększają, a powłoka stopniowo jaśnieje i przybiera typowy kolor chromu.
Może się też zdarzyć, że gęstość prądu jest zbyt wysoka. Zbyt duża gęstość prądu powoduje zbyt szybkie i nierównomierne osadzanie warstwy chromu, co również może skutkować ciemną lub czarną powierzchnią. Niższa gęstość prądu zapewnia bardziej równomierne tworzenie kryształów, a tym samym jaśniejszą i gładszą powłokę chromową. Należy tu znaleźć kompromis między szybkością a jakością.
Kolejnym ważnym czynnikiem jest to, że elektrolit mógł się zbyt mocno nagrzać z powodu wysokiej gęstości prądu. Zbyt wysoka temperatura również powoduje ciemnienie powłoki. W takim przypadku należy zmniejszyć gęstość prądu lub przerwać proces osadzania.
- Powłoka na stali nierdzewnej się nie trzyma
-
Jeśli powłoka na stali nierdzewnej się nie trzyma, najczęściej przyczyną jest niewystarczające przygotowanie powierzchni. Stal nierdzewna w kontakcie z powietrzem w ciągu kilku sekund tworzy niewidoczną warstwę tlenków, która chroni metal przed reakcjami chemicznymi, ale jednocześnie znacznie utrudnia przyczepność powłok.
Aby zapewnić trwałą powłokę, kluczowe jest przygotowanie elementu za pomocą procesu nickel strike. Ten aktywator galwaniczny usuwa warstwę tlenków oraz zawarty w stopie chrom, a następnie tworzy cienką warstwę niklu, do której kolejne powłoki dobrze się wiążą.
Alternatywnie można zastosować również gold strike (tzw. gold flash), aby uzyskać podobny efekt.
- Nikiel nie osadza się na żelazie
-
Potrzebna jest odrobina cierpliwości, ponieważ nikiel osadza się dość wolno. Możliwe, że gęstość prądu jest zbyt niska – wtedy proces potrwa znacznie dłużej. Należy jednak unikać zbyt dużej ilości pęcherzyków gazu, ponieważ mogą one powodować powstawanie czarnych smug.
Dużą wadą jest to, że powstawanie warstwy niklu jest trudne do zauważenia.
Sprawdź również jeszcze raz biegunowość anody – powinna być podłączona do plusa, a przedmiot poddawany powlekaniu do minusa.
- Opcje płatności
-
U nas możesz sfinalizować zakup za pomocą następujących metod płatności:
- ApplePay
- Bancontact
- Belfius
- EPS
- KBC
- Klarna
- Karta kredytowa
- PayPal
- Przedpłata (przelew bankowy)
Dostępne metody płatności mogą się różnić w zależności od kraju dostawy, używanej technologii, wybranych plików cookie lub zawartości koszyka.
- Informacje dotyczące wysyłki
-
Tutaj znajdziesz tabelę kosztów wysyłki.
W przypadku małych i lekkich przedmiotów możliwa jest wysyłka jako mała paczka (do 1 kg). Pamiętaj jednak, że opcja „Mała paczka” czasami może być dostarczana nieco dłużej. Standardowy czas dostawy w UE wynosi zwykle ok. 3–7 dni.
Kraj Wysyłka paczki Mała paczka Polska 12,00€ (ok. 51,40zł) 6,90€ (ok. 30zł)

